Информационные ресурсы и доступные данные, связанные с COVID-19

Установление новых показаний для разрешенных к медицинскому применению лекарств осуществляется с применением подходов in silico, in vitro и in vivo. Детальный анализ имеющихся в распоряжении исследователей экспериментальных и расчетных данных и извлечение из них полезной информации с применением методов машинного обучения позволяет выявлять перспективные направления поиска более безопасных и эффективных лекарственных средств. В данном разделе мы приводим регулярно пополняемую информацию относительно релевантных публикаций, веб-сервисов и иных связанных с COVID-19 сведений, которая используется для формирования гипотез при поиске новых фармакотерапевтических назначений используемых в клинической практике лекарственных препаратов.
Общие сведения о COVID-19
Интернет ресурсы содержащие общую информацию о COVID-19 репозиционировании препаратов
Релевантные Веб-ресурсы
Веб-сервисы и базы данных, содержащие специализированную информацию в отношении COVID-19
Избранные публикации
Подборка релевантных научных публикаций о результатах исследований и разработок, связанных с COVID-19
Патентная информация
Патенты на зарегистрированные лекарственные препараты, репозиционируемые для терапии COVID-19
Аналитические материалы
Анализ и фактографическая информация по различным аспектам, связанным с COVID-19
Мы постоянно прилагаем усилия по актуализации представленных данных. Заметили неточность? - Напишите нам, и мы внесем необходимые исправления. (Выберите интересующую вкладку ниже для получения более подробной информации)

Веб-ресурсы, веб-сервисы, базы данных и платформы создаваемый с целью обьединения информации о COVID-19 полученной из различных фармкомпаний, регионов и стран.
Коронавирус COVID–19: Официальная информация о коронавирусе в России
Официальная информация о ситуации с коронавирусной инфекцией в России. Оперативные данные.
Информационный центр ФармаCOVID
Информационный центр по вопросам фармакотерапии у пациентов с новой коронавирусной инфекцией COVID-19 на базе ФГБОУ ДПО РМАНПО МЗ РФ.
WHO: Coronavirus (COVID-19) Dashboard
ВОЗ: Статистика по заболеваемости COVID-19 в различных странах.
NCBI SARS-CoV-2 Resources
Компендиум ссылок на поисковую систему PubMed, полнотекстовый раздел PubMed Central (PMC), коллекцию статей LitCovid и Bookshelf содержащие информацию о SARS-CoV-2 (NCBI).
Centers for Disease Control and Prevention COVID-19 Data
Сведения о пандемии COVID-19 Центров по контролю и предотвращению заболеваний США.
CDC Museum COVID-19 Timeline
Временная привязка важных событий, связанных с пандемией COVID-19 (12.12.2019 - 06.07.2022).
Japan Pharmaceuticals and Medical Devices Agency. PMDA’s Efforts to Combat COVID-19
Информация о лечении COVID-19 Японского агентства по лекарствам и изделиям медицинского назначения.
Food & Drug Administration: Coronavirus (COVID-19)
Информация о терапии COVID-19 Управления по контролю качества пищевых продуктов и лекарственных препаратов США.
STIP COVID-19 Tracker: International Database on STI Policies
Интерактивная хронология политических инициатив, посвященных ответным мерам политики в области ответных мер на COVID-19.
Временные методические рекомендации Минздрава РФ (Версия 18 от 26.10.2023)
Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19).
VGARus (Virus Genome Aggregator of Russia)
Российская платформа агрегации информации о геномах вирусов разработанная ФБУН Центральном НИИ Эпидемиологии Роспотребнадзора.
WHO: Therapeutics and COVID-19: Living Guideline
ВОЗ: Информация о терапии COVID-19 (от 13 января 2023).
Cochrane COVID Reviews
Систематические обзоры исследований релевантных работ о COVID-19 относительно мер по контролю за распространением инфекции в Cochrane Library.
Cochrane Clinical Answers related to COVID-19
Ответы на вопросы по COVID-19 для клинических работников при оказании медицинской помощи.
COVID-19 Coronavirus Pandemic
Статистика по заболеваемости, смертности, выздоравливаемости COVID-19.
GISAID database: Rapid and Open Access to Epidemic and Pandemic Virus Data
Свободно-доступная база данных, содержащая сведения о вирусах, вызывающих эпидемии и пандемии.
Full-Text COVID-19 Guidelines and Reviews in Bookshelf (NLM)
"Книжная полка": Полнотекстовые аналитические обзоры, руководства и рекомендации по тематике COVID-19.
A Literature Hub for Tracking Up-To-Date Scientific Information About the Novel Coronavirus
Онлайн библиотека вышедших книжных изданий по COVID-19, содержащая ссылки на отобранные экспертами публикации.
The World Health Organisation (WHO): Coronavirus Disease (COVID-19) Pandemic
Сведения о пандемии COVID-19 Всемирной организации здравоохранения (ВОЗ), на русском языке.
WHO: COVID-19 Vaccine Tracker and Landscape
ВОЗ: Подробная информация о каждой разрабатываемой вакцине во всем мире, стадиях их разработки, он независимых организаций и государственных учреждений.
European COVID-19 Data Portal
Обьединенная Европейская платформа, направленная на сбор и всесторонний обмен данными доступных исследований о COVID-19 для мировых исследовательских сообществ.
European Medicines Agency: COVID-19 Treatments
Информация о терапии COVID-19 Европейского медицинского агентства.
Free full-text in PubMed Central (PMC) and the Public Health Emergency COVID-19 Initiative
Агрегация полнотекстовых публикаций о COVID-19 пятидесяти издательств на платформе PubMed Central.
COVID-19 Portfolio
Тщательно отобранные публикации связанные либо с COVID-19 и коронавирусом SARS-CoV-2.
CORDITE (CORona Drug InTEractions database)
Cведения о препаратах, взаимодействующих с белками вируса SARS-CoV-2 и человека, которые могут быть применены для терапии COVID-19.
SARS-CoV-2 Mutation Tracker: single mutations in hCoV-19 Genomes
Онлайн статистика сведений о мутантных формах и мутациях SARS-Cov-2 основанная на всемирных данных.

Общие веб-ресурсы

Веб-ресурсы, веб-сервисы, базы данных и платформы создаваемый с целью обьединения информации о COVID-19 полученной из различных фармкомпаний, регионов и стран.
ChEMBL Database
База данных по биологически-активным соединением Европейского института биоинформатики ChEMBL.
COVID-19 Data Portal
Единая Европейская платформа по COVID-19 на базе разных источников европейских и мировых исследовательских сообществ.
IUPHAR/BPS Guide to PHARMACOLOGY
Информация о COVID-19, подготовленная Международным союзом по фундаментальной и клинической фармакологии (IUPHAR).
DrugBank
Информация о 500 тыс. лекарств, мишенях и фармацевтических продуктах, включая информацию о COVID-19.
UniProtKB Knowledgebase
База знаний по белкам Европейского института биоинформатики, содержащая информацию о COVID-19.
WHO COVID-19 Research Database
База данных по исследованиям COVID-19, подготовленная Всемирной организацией здравоохранения (ВОЗ).
Protein Data Bank
База данных пространстенных структур биомакромолекул и их комплексов с лигандами Protein Data Bank, включая данныею о COVID-19.
EMBL & COVID-19
Европейская платформа информации по COVID-19, подготовленной Европейской лабораторией молекулярной биологии (EMBL).
National Institutes of Health COVID-19 Research
Информационные ресурсы по COVID-19 представленные Национальными институтами здоровья (NIH) США.
Специализированные веб-ресурсы

Веб-ресурсы, веб-сервисы, базы данных и платформы специлизированно выделенные и посвященные проблематике COVID-19.
ACovPepDB
База данных по антикоронавирусным пептидам (514 документов с информацией о 214 уникальных пептидах).
COVID-19 OpenData Portal
Информационный ресурс, содержащий данные по борьбе с COVID-19, Национального центра передовых трансляционных исследований Национальных институтов здоровья (NCATS NIH) США.
A collection of COVID19 related data presented in BindingDB
Сведения по антикоронавирусным соединениям (SARS, MERS, SARS-CoV-2) в базе данных BindingDB.
COVID19db
Платформа для поиска лекарств против COVID-19 c применением транскриптомных данных, интегрирующая информацию о 39 930 взаимодействиях между 2 037 лекарственых препаратах, 1 116 мишенях и 207 регуляторных сигнальных путях.
Liverpool COVID-19 Drug Interaction Checker
Веб-ресурс по оценке межлекарственных взаимодействий препаратов, используемых для терапии COVID-19.
PostEra SARS-CoV protease inhibitors data
Веб-ресурс содержащий сведения по молекулярному дизайну, синтезу и результатам тестирования фарамкологических веществ, ингибирующих главную протеазу 3CLpro SARS-CoV-2.
COVID-19 (Coronavirus Disease 2019) data in PubChem
Информация об антикоронавирусных соединениях и картах заболеваний COVID-19 в базе данных NCBI PubChem.
CoREx (The COVID-19 Repositioning Explorer)
Веб-ресурс по репозиционированию лекарственных препаратов против COVID-19, обеспечивающий визуализацию разрешенных FDA препаратов в контексте их белковых мишеней, некоторых доступных интерактомов и функции соответствующих белков.
2020

1. Li G., De Clercq E. (2020) Therapeutic options for the 2019 novel coronavirus (2019-nCoV) // Nat. Rev. Drug Discov. V.19. No. 3. P. 149-150. DOI: 10.1038/d41573-020-00016-0
2. Hoffmann M., Kleine-Weber H., Schroeder S. et al. (2020) SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor // Cell. V. 181. No. 2. P. 271-280. DOI: 10.1016/j.cell.2020.02.052
3. Beigel J.H., Tomashek K.M., Dodd L.E. et al. (2020) Remdesivir for the Treatment of Covid-19 - Final Report // N. Engl. J, Med. V. 383. No. 19. P. 1813-1826. DOI: 10.1056/NEJMoa2007764
4. Yan R., Zhang Y., Li Y., Xia L., Guo Y., Zhou Q. (2020) Structural basis for the recognition of SARS-CoV-2 by full-length human ACE2 // Science. V. 367. No. 6485. P. 1444-1448. DOI: 10.1126/science.abb2762
5. Tay M.Z., Poh C.M., Rénia L., MacAry P.A., Ng L.F.P. (2020) The trinity of COVID-19: immunity, inflammation and intervention // Nat. Rev. Immunol. V. 20. No. 6. P. 363-374. DOI: 10.1038/s41577-020-0311-8
6. Shang J., Ye G., Shi K. et al. (2020) Structural basis of receptor recognition by SARS-CoV-2 // Nature. V. 581. No. 7807. P. 221-224. DOI: 10.1038/s41586-020-2179-y
7. Chu D.K., Akl E.A., Duda S. et al. (2020) Physical distancing, face masks, and eye protection to prevent person-to-person transmission of SARS-CoV-2 and COVID-19: a systematic review and meta-analysis // Lancet. V. 395. No. 10242. P. 1973-1987. DOI: 10.1016/S0140-6736(20)31142-9
8. Jin Z., Du X., Xu Y. et al. (2020) Structure of Mpro from SARS-CoV-2 and discovery of its inhibitors // Nature. V. 582. No. 7811. P. 289-293. DOI: 10.1038/s41586-020-2223-y
9. Chen Y., Liu Q., Guo D. (2020) Emerging coronaviruses: Genome structure, replication, and pathogenesis // J. Med. Virol. V. 92. No. 4. P. 418-423. DOI: 10.1002/jmv.25681
10. Bikdeli B., Madhavan M..V, Jimenez D. et al. (2020) COVID-19 and Thrombotic or Thromboembolic Disease: Implications for Prevention, Antithrombotic Therapy, and Follow-Up: JACC State-of-the-Art Review // J. Am. Coll. Cardiol. V. 75. No. 23. P. 2950-2973. DOI: 10.1016/j.jacc.2020.04.031
11. Zhang L., Lin D., Sun X. et al. (2020) Crystal structure of SARS-CoV-2 main protease provides a basis for design of improved α-ketoamide inhibitors // Science. V. 368. No. 6489. P. 409-412. DOI: 10.1126/science.abb3405
12. Wang Q., Zhang Y., Wu L. et al. (2020) Structural and Functional Basis of SARS-CoV-2 Entry by Using Human ACE2 // Cell. V. 181. No. P. 894-904. DOI: 10.1016/j.cell.2020.03.045
13. Shang J., Wan Y., Luo C. et al. (2020) Cell entry mechanisms of SARS-CoV-2 // Proc. Natl. Acad. Sci. U S A. V. 117. No. 21. P. 11727-11734. DOI: 10.1073/pnas.2003138117
14. Gordon D.E., Jang G.M., Bouhaddou M. et al. (2020) A SARS-CoV-2 protein interaction map reveals targets for drug repurposing // Nature. V. 583. No. 7816. P. 459-468. DOI: 10.1038/s41586-020-2286-9
15. Zhang H., Penninger J.M., Li Y., Zhong N., Slutsky A.S. (2020) Angiotensin-converting enzyme 2 (ACE2) as a SARS-CoV-2 receptor: molecular mechanisms and potential therapeutic target // Intensive Care Med. V. 46. No. 4. P.586-590. DOI: 10.1007/s00134-020-05985-9
16. Sungnak W., Huang N., Bécavin C. et al. (2020) HCA Lung Biological Network. SARS-CoV-2 entry factors are highly expressed in nasal epithelial cells together with innate immune genes // Nat. Med. V. 26. No. 5. P. 681-687. DOI: 10.1038/s41591-020-0868-6
17. Connors J.M., Levy J.H. (2020) COVID-19 and its implications for thrombosis and anticoagulation // Blood. V. 135. No. 23. P. 2033-2040. DOI: 10.1182/blood.2020006000
18. Guy R.K. DiPaola R.S., Romanelli F., Dutch R.E. (2020) Rapid repurposing of drugs for COVID-19 // Science. V. 368. No. 6493 P.829-830. DOI: 10.1126/science.abb9332
19. Li Z., Li X., Huang Y.Y. et al. (2020) Identify potent SARS-CoV-2 main protease inhibitors via accelerated free energy perturbation-based virtual screening of existing drugs // Proc. Natl. Acad. Sc.i U S A. V. 117. No. 44. P. 27381-27387. DOI: 10.1073/pnas.2010470117
20. Monteil V., Kwon H., Prado P. et al. (2020) Inhibition of SARS-CoV-2 Infections in Engineered Human Tissues Using Clinical-Grade Soluble Human ACE2. Cell. V. 181. No. 4. P. 905-913.e7. DOI: 10.1016/j.cell.2020.04.004
21. Moore J.B., June C.H. (2020) Cytokine release syndrome in severe COVID-19 // Science. V. 368. No. 6490. P. 473-474. DOI: 10.1126/science.abb8925
22. Rambaut A., Holmes E.C., O'Toole Á. et al. (2020) A dynamic nomenclature proposal for SARS-CoV-2 lineages to assist genomic epidemiology. // Nat. Microbiol. V. 5. No. 11. P. 1403-1407. DOI: 10.1038/s41564-020-0770-5
23. Kim D., Lee J.Y., Yang J.S., Kim J.W., Kim V.N., Chang H. (2020) The Architecture of SARS-CoV-2 Transcriptome // Cell. V. 181. No. 4. P. 914-921.e10. doi: 10.1016/j.cell.2020.04.011. DOI: 10.1016/j.cell.2020.04.011
24. Puelles V.G., Lütgehetmann M., Lindenmeyer M.T. et al. (2020) Multiorgan and Renal Tropism of SARS-CoV-2. N Engl J Med. 2020 Aug 6;383(6):590-592. doi: 10.1056/NEJMc2011400 // N. Engl. J. Med. V. 383. No. 6. P. 590-592. doi: 10.1056/NEJMc2011400. DOI: 10.1056/NEJMc2011400
25. Thanh Le T., Andreadakis Z., Kumar A. et al. (2020) The COVID-19 vaccine development landscape // Nat. Rev. Drug Discov. V. 19. No. 5. P. 305-306. DOI: 10.1038/d41573-020-00073-5
26. Tai W., He L., Zhang X. et al. (2020) Trimeric receptor-binding domain of SARS-CoV-2 acts as a potent inhibitor of ACE2 receptor-mediated viral entry // Cell. Mol. Immunol. V. 17. No. 6. P. 613-620. DOI: 10.1038/s41423-020-0400-4
27. Ju B., Zhang Q., Ge J. et al. (2020) Human neutralizing antibodies elicited by SARS-CoV-2 infection // Nature. V. 584. No. 7819. P. 115-119. DOI: 10.1038/s41586-020-2380-z
28. Gao Y., Yan L., Huang Y. et al. (2020) Structure of the RNA-dependent RNA polymerase from COVID-19 virus // Science. V. 368. No. 6492. P. 779-782. DOI: 10.1126/science.abb7498
29. Cantuti-Castelvetri L., Ojha R., Pedro L.D. et al. (2020) Neuropilin-1 facilitates SARS-CoV-2 cell entry and infectivity // Science. V. 370. No. 6518. P. 856-860. DOI: 10.1126/science.abd2985
30. Huang Y., Yang C., Xu X.F., Xu W., Liu S.W. (2020) Structural and functional properties of SARS-CoV-2 spike protein: potential antivirus drug development for COVID-19 // Acta Pharmacol. Sin. V. 41. No. 9. P. 1141-1149. DOI: 10.1038/s41401-020-0485-4
31. Zarocostas J. (2020) How to fight an infodemic // Lancet. V. 395. No. 10225. P. 676. DOI: 10.1016/S0140-6736(20)30461-X
32. Gupta A., Madhavan M.V., Sehgal K. et al. (2020) Extrapulmonary manifestations of COVID-19 // Nat. Med. V. 26. No. 7. P. 1017-1032. DOI: 10.1038/s41591-020-0968-3
33. Li Q., Wu J., Nie J. et al. (2020) The Impact of Mutations in SARS-CoV-2 Spike on Viral Infectivity and Antigenicity // Cell. V. 182, No. 5. P. 1284-1294.e9. DOI: 10.1016/j.cell.2020.07.012
34. Riva L., Yuan S., Yin X. et al. (2020) Discovery of SARS-CoV-2 antiviral drugs through large-scale compound repurposing // Nature. V. 586. No. 7827. P. 113-119. DOI: 10.1038/s41586-020-2577-1
35. Gil C., Ginex T., Maestro I. et al. (2020) COVID-19: Drug Targets and Potential Treatments // J. Med. Chem. V. 63. No. 21. P. 12359-12386. DOI: 10.1021/acs.jmedchem.0c00606
36. Dong L., Hu S., Gao J. (2020) Discovering drugs to treat coronavirus disease 2019 (COVID-19) // Drug Discov. Ther. V. 14. No. 1. P. 58-60. DOI: 10.5582/ddt.2020.01012
37. Touret F., Gilles M., Barral K. et al. (2020) In vitro screening of a FDA approved chemical library reveals potential inhibitors of SARS-CoV-2 replication // Sci. Rep. V. 10. P. 13093. DOI: 10.1038/s41598-020-70143-6
38. Zhu W., Xu M., Chen C.Z. et al. (2020) 3CL Protease Inhibitors by a Quantitative High-Throughput Screening // ACS Pharmacol. Transl. Sci. V. 3. No. 5. P. 1008-1016. DOI: 10.1021/acsptsci.0c00108
39. Watanabe Y., Allen J.D., Wrapp D., McLellan J.S., Crispin M. (2020) Site-specific glycan analysis of the SARS-CoV-2 spike // Science. V. 369. No. 6501. P. 330-333. DOI: 10.1126/science.abb9983
40. Weston S., Coleman C.M., Haupt R. et al. (2020) Broad Anti-coronavirus Activity of Food and Drug Administration-Approved Drugs against SARS-CoV-2 In Vitro and SARS-CoV In Vivo // J. Virol. V. 94. No. 21. P. e01218-20. DOI: 10.1128/JVI.01218-20
41. Dai W., Zhang B., Jiang X.M. et al. (2020) Structure-based design of antiviral drug candidates targeting the SARS-CoV-2 main protease // Science. V. 368. No. 6497. P. DOI: 10.1126/science.abb4489
42. Sadegh S., Matschinske J., Blumenthal D.B. et al. (2020) Exploring the SARS-CoV-2 virus-host-drug interactome for drug repurposing // Nat. Commun. V. 11. P. 3518. DOI: 10.1038/s41467-020-17189-2
43. Pizzorno A., Padey B., Dubois J. et al. (2021) In vitro evaluation of antiviral activity of single and combined repurposable drugs against SARS-CoV-2 // Antiviral Res. V. 181. P. 104878. DOI: 10.1016/j.antiviral.2020.104878
44. Singh N., Decroly E., Khatib A.M., Villoutreix B.O. (2020) Structure-based drug repositioning over the human TMPRSS2 protease domain: search for chemical probes able to repress SARS-CoV-2 Spike protein cleavages // Eur. J. Pharm. Sci. V. 153. P. 105495. DOI: 10.1016/j.ejps.2020.105495
45. Matsuyama S., Nao N., Shirato K. et al. (2020) Enhanced isolation of SARS-CoV-2 by TMPRSS2-expressing cells // Proc. Natl. Acad. Sci. U S A. V. 117. No. 13. P. 7001-7003. DOI: 10.1073/pnas.2002589117
46. Stroylov V.S., Svitanko I.V. (2020) Computational identification of disulfiram and neratinib as putative SARS-CoV-2 main protease inhibitors // Mendeleev Communications. V. 30. No. 4. P. 419-420. DOI: 10.1016/j.mencom.2020.07.004
47. Nersisyan S., Shkurnikov M., Turchinovich A. et al. (2020) Integrative analysis of miRNA and mRNA sequencing data reveals potential regulatory mechanisms of ACE2 and TMPRSS2 // PLoS One. V. 15. P. :e0235987. DOI: 10.1371/journal.pone.0235987
48. Nasonov E., Samsonov M. The role of Interleukin 6 inhibitors in therapy of severe COVID-19 // Biomed. Pharmacother. V. 131. P. 110698. DOI: 10.1016/j.biopha.2020.110698
49. Новиков Ф.Н. , Стройлов В.С. , Свитанько И.В. , Небольсин В.Е. (2020) Молекулярные основы патогенеза COVID-19 // Успехи химии. Т. 89. С. 858-878. DOI: 10.1070/RCR4961
50. Ionov N., Pogodin P., Poroikov V. (2029) Assessing the Prediction Quality of the Anti-SARS-CoV-2 Activity Using the D3Targets-2019-nCoV Web Service // Biomedical Chemistry: Research and Methods. V. 3. No. 4. P. e00140. DOI: 10.18097/BMCRM00140
51. Гомазков О.А. (2020) Эндотелий - мишень, которую выбирает коронавирус. Анализ молекулярных и патофизиологических механизмов COVID-19 // Москва: Из-во ИКАР. - 62 С. Ссылка
52. Скворцов В.С., Дружиловский Д.С., Веселовский А.В. (2020) Потенциальные ингибиторы протеазы 3СLpro вируса COVID-19: репозиционирование лекарств // Biomedical Chemistry: Research and Methods. Т. 3. С. e00124. DOI: 10.18097/BMCRM00124
53. Фисенко В.П., Чичкова Н.В. (2020) Современная пандемия COVID-19 и лекарственные средства // Экспериментальная и клиническая фармакология. Т. 83. С. 43-44. DOI: 10.30906/0869-2092-2020-83-4-43-44
2021

1. Chen C.Z., Shinn P., Itkin Z. et al. (2021) Drug repurposing screen for compounds inhibiting the cytopathic effect of SARS-CoV-2 // Front. Pharmacol. V. 11. P. 592737. DOI: 10.3389/fphar.2020.592737
2. MacRaild C.A., Mohammed M.U., Faheem, Murugesan S. et al. (2022) Systematic down-selection of repurposed drug candidates for COVID-19 // Int. J. Mol. Sci. V. 23. No. 19. P. 11851. DOI: 10.3390/ijms231911851
3. Hanson Q.M., Wilson K.M., Shen M., et al. (2020) Targeting ACE2-RBD Interaction as a Platform for COVID-19 Therapeutics: Development and Drug-Repurposing Screen of an AlphaLISA Proximity Assay // ACS Pharmacol. Transl. Sci. V. 3. No. 6. P. 1352-1360. Published 2020 Nov 17. DOI: 10.1021/acsptsci.0c00161
4. WHO Solidarity Trial Consortium; Pan H., Peto R., Henao-Restrepo A.M. et al. (2021) Repurposed Antiviral Drugs for Covid-19 - Interim WHO Solidarity Trial Results // N. Engl. J. Med. V. 384. No. 6. P. 497-511. DOI: 10.1056/NEJMoa2023184
5. Zhao L., Li S., Zhong W. (2022) Mechanism of action of small-molecule agents in ongoing clinical trials for SARS-CoV-2: A review // Front. Pharmacol. V. 13. P. 840639. DOI: 10.3389/fphar.2022.840639
6. Nalbandian A., Sehgal K., Gupta A. et al. (2021) Post-acute COVID-19 syndrome // Nat. Med. 2021 Apr;27(4):601-615. DOI: 10.1038/s41591-021-01283-z
7. Harvey W.T., Carabelli A.M., Jackson B. et al. (2021) SARS-CoV-2 variants, spike mutations and immune escape // Nat. Rev. Microbiol. V. 19. No. 7. P. 409-424. DOI: 10.1038/s41579-021-00573-0
8. V'kovski P., Kratzel A., Steiner S., Stalder H., Thiel V. (2021) Coronavirus biology and replication: implications for SARS-CoV-2 // Nat. Rev. Microbiol. V. 19. No. 3. P.155-170. DOI: 10.1038/s41579-020-00468-6
9. Hu B., Guo H., Zhou P., Shi Z.L. (2021) Characteristics of SARS-CoV-2 and COVID-19 // Nat Rev Microbiol. V. 19. No. 3. P. 141-154. DOI: 10.1038/s41579-020-00459-7
10. Lopez-Leon S., Wegman-Ostrosky T., Perelman,C. et al. (2021) More than 50 long-term effects of COVID-19: a systematic review and meta-analysis // Sci. Rep. V. 11. P. 16144. DOI: 10.1038/s41598-021-95565-8
11. Kemp S.A., Collier D.A., Datir R.P. et al. (2021) SARS-CoV-2 evolution during treatment of chronic infection // Nature. V. 592. No. 7853. P. 277-282. DOI: 10.1038/s41586-021-03291-y
12. Owen D.R., Allerton .CM.N., Anderson A.S. et al. (2021) An oral SARS-CoV-2 Mpro inhibitor clinical candidate for the treatment of COVID-19 // Science. V. 374. No. 6575. P. 1586-1593. DOI: 10.1126/science.abl4784
13. Tao K., Tzou P.L., Nouhin J. et al. (2021) The biological and clinical significance of emerging SARS-CoV-2 variants // Nat. Rev. Genet. V. 22. No. 12. P. 757-773. DOI: 10.1038/s41576-021-00408-x
14. Nelde A., Bilich T., Heitmann J.S. et al. (2021) SARS-CoV-2-derived peptides define heterologous and COVID-19-induced T cell recognition // Nat, Immunol. V. 22. P. 74-85. DOI: 10.1038/s41590-020-00808-x
15. Yong S.J. (2021) Long COVID or post-COVID-19 syndrome: putative pathophysiology, risk factors, and treatments // Infect Dis (Lond). V. 53. No. 10. P. 737-754. DOI: 10.1080/23744235.2021
16. Kokic G., Hillen H.S., Tegunov D. et al. (2021) Mechanism of SARS-CoV-2 polymerase stalling by remdesivir // Nat. Commun. V. 12. No. 1. P. 279. DOI: 10.1038/s41467-020-20542-0
17. Han Y., Duan X., Yang L. et al. (2021) Identification of SARS-CoV-2 inhibitors using lung and colonic organoids // Nature. V. 589. No. 7841. P. 270-275. DOI: 10.1038/s41586-020-2901-9
18. Kabinger F., Stiller .C, Schmitzová J. et al. (2021) Mechanism of molnupiravir-induced SARS-CoV-2 mutagenesis // Nat. Struct. Mol. Biol. V. 28. No. 9. P. 740-746. DOI: 10.1038/s41594-021-00651-0
19. Osuchowski M.F., Winkler M.S., Skirecki T. et al. (2021) The COVID-19 puzzle: deciphering pathophysiology and phenotypes of a new disease entity // Lancet Respir. Med. V. 9. No. 6. P. 622-642. DOI: 10.1016/S2213-2600(21)00218-6
20. Braga L., Ali H., Secco I. et al. (2021) Drugs that inhibit TMEM16 proteins block SARS-CoV-2 spike-induced syncytia // Nature. V. 594. No. 7861. P. 88-93. DOI: 10.1038/s41586-021-03491-6
21. Stukalov A., Girault V., Grass V. et al. (2021) Multilevel proteomics reveals host perturbations by SARS-CoV-2 and SARS-CoV // Nature. V. 594. No. 7862. P. 246-252. DOI: 10.1038/s41586-021-03493-4
22. Qiao J., Li Y.S., Zeng R. et al. (2021) SARS-CoV-2 Mpro inhibitors with antiviral activity in a transgenic mouse model // Science. V. 371. No. 6536. P. 1374-1378. DOI: 10.1126/science.abf1611
23. Jones I,, Roy P. (2021) Sputnik V COVID-19 vaccine candidate appears safe and effective // Lancet. V. 397. No. 10275. P. 642-643. DOI: 10.1016/S0140-6736(21)00191-4
24. Osipiuk J., Azizi S.A., Dvorkin, S. et al. (2021) Structure of papain-like protease from SARS-CoV-2 and its complexes with non-covalent inhibitors // Nat. Commun. V. 12. P. 743. DOI: 10.1038/s41467-021-21060-3
25. Rhea E.M., Logsdon A.F., Hansen K.M. et al. (2021) The S1 protein of SARS-CoV-2 crosses the blood-brain barrier in mice // Nat. Neurosci. V. 24. No. 3. P. 368-378. DOI: 10.1038/s41593-020-00771-8
26. Dejnirattisai W., Zhou D., Ginn H.M. et al. (2021) The antigenic anatomy of SARS-CoV-2 receptor binding domain // Cell. V. 184. No. 8. P. 2183-2200.e22. DOI: 10.1016/j.cell.2021.02.032
27. Zahradník J., Marciano S., Shemesh M. et al. (2021) SARS-CoV-2 variant prediction and antiviral drug design are enabled by RBD in vitro evolution // Nat. Microbiol. V. 6. No. 9. P. 1188-1198. DOI: 10.1038/s41564-021-00954-4
28. Dittmar M., Lee J.S., Whig K. et al. (2021) Drug repurposing screens reveal cell-type-specific entry pathways and FDA-approved drugs active against SARS-Cov-2 // Cell Rep. 2021. V. 35. No. 1. P. 108959. DOI: 10.1016/j.celrep.2021.108959
29. Günther S., Reinke P.Y.A., Fernández-García Y. et al. (2021) X-ray screening identifies active site and allosteric inhibitors of SARS-CoV-2 main protease // Science. V. 372. No. 6542. P. 642-646. DOI: 10.1126/science.abf7945
30. Kuo C.J., Chao T.L., Kao H.C. et al. (2021) Kinetic Characterization and Inhibitor Screening for the Proteases Leading to Identification of Drugs against SARS-CoV-2 // Antimicrob Agents Chemother. V. 65. No. 4. e02577-20. Published 2021 Mar 18. DOI: 10.1128/AAC.02577-20
31. Kuzikov M., Costanzi E., Reinshagen J. et al. (2021) Identification of Inhibitors of SARS-CoV-2 3CL-Pro Enzymatic Activity Using a Small Molecule in Vitro Repurposing Screen // ACS Pharmacol Transl Sci. V. 4. No. 3. 1096-1110. DOI: 10.1021/acsptsci.0c00216
32. Tompa D.R., Immanuel A., Srikanth S., Kadhirvel S. (2021) Trends and strategies to combat viral infections: A review on FDA approved antiviral drugs // Int. J. Biol. Macromol. V. 172. P. 524-541. DOI: 10.1016/j.ijbiomac.2021.01.076
33. Ren X., Wen W., Fan X. et al. (2021) COVID-19 immune features revealed by a large-scale single-cell transcriptome atlas // Cell. V. 184. No. 7. P. 1895-1913.e19. DOI: 10.1016/j.cell.2021.01.053
34. Tummino T.A., Rezelj V.V., Fischer B. et al. (2021) Drug-induced phospholipidosis confounds drug repurposing for SARS-CoV-2 // Science. V. 373. No. 6554. P. 541-547. DOI: 10.1126/science.abi4708
35. Jan J.T., Cheng T.R., Juang Y.P. (2021) Identification of existing pharmaceuticals and herbal medicines as inhibitors of SARS-CoV-2 infection // Proc. Natl. Acad. Sci. U S A. V. 118. P. e2021579118. DOI: 10.1073/pnas.2021579118
36. Jang W.D., Jeon S., Kim S., Lee S.Y. (2021) Drugs repurposed for COVID-19 by virtual screening of 6,218 drugs and cell-based assay // Proc. Natl. Acad. Sc.i U S A. V. 118. P. e2024302118. DOI: 10.1073/pnas.2024302118
37. Muratov E.N. , Amaro R. , Andrade C.H. et al. (2021) A critical overview of computational approaches employed for COVID-19 drug discovery // Chem. Soc. Rev. V. 50. No. 16. P. 9121-9151. DOI: 10.1039/d0cs01065k
38. Al-Aly Z., Xie Y., Bowe B. (2021) High-dimensional characterization of post-acute sequelae of COVID-19 // Nature. V. 594. No. 7862. P. 259-264. DOI: 10.1038/s41586-021-03553-9
39. Bakowski M.A., Beutler N., Wolff K.C. et al. (2021) Drug repurposing screens identify chemical entities for the development of COVID-19 interventions // Nat. Commun. V. 12. P. 3309. DOI: 10.1038/s41467-021-23328-0
40. Mirabelli C., Wotring J.W., Zhang C.J. (2021) Morphological cell profiling of SARS-CoV-2 infection identifies drug repurposing candidates for COVID-19 // Proc. Natl. Acad. Sci. U S A. V. 118. P. e2105815118. DOI: 10.1073/pnas.2105815118
41. Schloer S., Brunotte L., Mecate-Zambrano A. et al. (2021) Drug synergy of combinatory treatment with remdesivir and the repurposed drugs fluoxetine and itraconazole effectively impairs SARS-CoV-2 infection in vitro // Br. J. Pharmacol. V. 178. P. 2339-2350. DOI: 10.1111/bph.15418
42. Shyr Z.A., Cheng Y.S., Lo D.C., Zheng W. (2021) Drug combination therapy for emerging viral diseases // Drug Discov. Today. V. 26. P. 2367-2376. DOI: 10.1016/j.drudis.2021.05.008
43. Ng Y.L., Salim C.K., Chu J.J.H. (2021) Drug repurposing for COVID-19: Approaches, challenges and promising candidates // Pharmacol. Ther. V. 228. P. 107930. DOI: 10.1016/j.pharmthera.2021
44. Smith P.F., Dodds M., Bentley D., Yeo K., Rayner C. (2021) Dosing will be a key success factor in repurposing antivirals for COVID-19 // Br. J. Clin. Pharmacol. V. 87. P. 3451-3454. DOI: 10.1111/bcp.14314
45. Chugh H., Awasthi A., Agarwal Y. et al. (2021) A comprehensive review on potential therapeutics interventions for COVID-19 // Eur. J. Pharmacol. V. 890. P. 173741. DOI: 10.1016/j.ejphar.2020.173741
46. Terracciano R., Preianò M., Fregola A. et al. (2021) Mapping the SARS-CoV-2-Host Protein-Protein Interactome by Affinity Purification Mass Spectrometry and Proximity-Dependent Biotin Labeling: A Rational and Straightforward Route to Discover Host-Directed Anti-SARS-CoV-2 Therapeutics // Int. J. Mol. Sci. V. 22. P. DOI: 10.3390/ijms22020532
47. Chu J., Xing C., Du Y. et al. (2021) Pharmacological inhibition of fatty acid synthesis blocks SARS-CoV-2 replication // Nat. Metab. V. 3. P. 1466-1475. DOI: 10.1038/s42255-021-00479-4
48. Yuce M., Cicek E., Inan T. et al. (2021) Repurposing of FDA-approved drugs against active site and potential allosteric drug-binding sites of COVID-19 main protease // Proteins. V. 89. P. 1425-1441. DOI: 10.1002/prot.26164
49. Zeng J., Weissmann F., Bertolin A.P. et al. (2021) Identifying SARS-CoV-2 antiviral compounds by screening for small molecule inhibitors of nsp13 helicase // Biochem. J. V. 478. P. 2405-2423. DOI: 10.1042/BCJ20210201
50. Kreutzberger A.J.B., Sanyal A., Ojha R. et al. (2021) Synergistic Block of SARS-CoV-2 Infection by Combined Drug Inhibition of the Host Entry Factors PIKfyve Kinase and TMPRSS2 Protease // J. Virol. V. 95. P. e0097521. DOI: 10.1128/JVI.00975-21
51. Macip G., Garcia-Segura P., Mestres-Truyol J. et al. (2021) Haste makes waste: A critical review of docking-based virtual screening in drug repurposing for SARS-CoV-2 main protease (M-pro) inhibition // Med. Res. Rev. V. 42. P. 744-769. DOI: 10.1002/med.21862
52. Wong K.K., Lee S.W.H., Kua K.P. (2021) N-Acetylcysteine as Adjuvant Therapy for COVID-19 - A Perspective on the Current State of the Evidence // J. Inflamm. Res. V. 6. P. 2993-3013. DOI: 10.2147/JIR.S306849
53. Desantis J., Mercorelli B., Celegato M. et al. (2021) Indomethacin-based PROTACs as pan-coronavirus antiviral agents // Eur. J. Med. Chem. V. 226. P. 113814. DOI: 10.1016/j.ejmech.2021.113814
54. Vique-Sánchez J.L. (2021) Potential inhibitors interacting in Neuropilin-1 to develop an adjuvant drug against COVID-19, by molecular docking // Bioorg. Med. Chem. V. 33. P. 116040. DOI: 10.1016/j.bmc.2021.116040
55. Biering S.B., Van Dis E., Wehri E. et al. (2021) Screening a Library of FDA-Approved and Bioactive Compounds for Antiviral Activity against SARS-CoV-2 // ACS Infect. Dis. V. 7. P.2337-2351. DOI: 10.1021/acsinfecdis.1c00017
56. Eberle R.J., Olivier D.S., Amaral M.S. et al. (2021) The Repurposed Drugs Suramin and Quinacrine Cooperatively Inhibit SARS-CoV-2 3CLpro In Vitro // Viruses. V. 13. P. 873. DOI: 10.3390/v13050873
57. Fu W., Chen Y., Wang K. et al. (2021) Repurposing FDA-approved drugs for SARS-CoV-2 through an ELISA-based screening for the inhibition of RBD/ACE2 interaction // Protein Cell. V. 12. P. 586-591. DOI: 10.1007/s13238-020-00803-w
58. Lin M., Dong H.Y., Xie H.Z., Li Y.M., Jia L. (2021) Why do we lack a specific magic anti-COVID-19 drug? Analyses and solutions // Drug Discov.Today. V. 26. P. 631-636. DOI: 10.1016/j.drudis.2020.12.010
59. Zakharova M.Y., Kuznetsova A.A., Uvarova V.I. et al. (2021) Pre-Steady-State Kinetics of the SARS-CoV-2 Main Protease as a Powerful Tool for Antiviral-Drug Discovery // Front. Pharmacol. V. 12, P. 773198. DOI: 10.3389/fphar.2021.773198
60.Kozlovskaya L.I., Piniaeva A.N., Ignatyev G.M. et al. (2021) Long-term humoral immunogenicity, safety and protective efficacy of inactivated vaccine against COVID-19 (CoviVac) in preclinical studies // Emerg. Microbes Infect. V. 10. No. 1. P. 1790-1806. DOI: 10.1080/22221751.2021.1971569
61. Savosina P.I., Druzhilovskiy D.S., Poroikov V.V. (2021) COVID-19: Analysis of drug repositioning practice // Pharmaceutical Chemistry Journal. V. 54. P. 989-996. DOI: 10.1007/s11094-021-02308-0
62. Zhuravel S.V., Khmelnitskiy O.K., Burlaka O.O. et al. (2021) Nafamostat in hospitalized patients with moderate to severe COVID-19 pneumonia: a randomised Phase II clinical trial // EClinicalMedicine. V. 41. P. 101169. DOI: 10.1016/j.eclinm.2021.101169
63. Letarov A.V., Babenko V.V., Kulikov E.E. (2021) Free SARS-CoV-2 Spike Protein S1 Particles May Play a Role in the Pathogenesis of COVID-19 Infection // Biochemistry (Mosc). V. 86. P. 257-261. DOI: 10.1134/S0006297921030032
64. Sulimov V.B., Kutov D.C., Taschilova A.S. et al. (2021) Docking Paradigm in Drug Design // Curr Top Med Chem. V. 21. P. 507-546. DOI: 10.2174/1568026620666201207095626
65. Zarubin A., Stepanov V., Markov A. et al. (2021) Structural Variability, Expression Profile, and Pharmacogenetic Properties of TMPRSS2 Gene as a Potential Target for COVID-19 Therapy // Genes (Basel). V. 12. P. 19. DOI: 10.3390/genes12010019
66. Poloznikov A.A., Nersisyan S.A., Hushpulian D.M. et al. (2021) HIF Prolyl Hydroxylase Inhibitors for COVID-19 Treatment: Pros and Cons // Front Pharmacol. V. 11. P. 621054. DOI: 10.3389/fphar.2020.621054
67. Melikhov O., Kruglova T., Lytkina K. et al. (2021) Use of Janus kinase inhibitors in COVID-19: a prospective observational series in 522 individuals // Ann Rheum Dis. V. 80. P. 1245-1246. DOI: 10.1136/annrheumdis-2021-220049
68. Kozlovskaya L.I., Volok V.P., Shtro A.A. et al. (2021) Phenoxazine nucleoside derivatives with a multiple activity against RNA and DNA viruses // Eur. J. Med. Chem. V. 220. P. 113467. DOI: 10.1016/j.ejmech.2021.113467
69. Leneva I., Kartashova N., Poromov A. et al. (2021) Antiviral Activity of Umifenovir In Vitro against a Broad Spectrum of Coronaviruses, Including the Novel SARS-CoV-2 Virus // Viruses. V. 13. P. 1665. DOI: 10.3390/v13081665
70. Holms R.D., Ataullakhanov R.I. (2021) Ezrin Peptide Therapy from HIV to COVID: Inhibition of Inflammation and Amplification of Adaptive Anti-Viral Immunity // Int. J. Mol. Sci. V. 22. P. 11688. DOI: 10.3390/ijms222111688
71. Гомазков О.А. (2021) COVID-19. Патогенез сосудистых поражений, или Дьявол кроется в деталях // Москва: Из-во ИКАР. - 72 С. Ссылка
72. Гомазков О.А. (2021) КОВИД-19. Клеточные и молекулярные механизмы поражения мозга // Успехи современной биологии. Т. 141. № 5. С. 457-466. DOI: 10.31857/S0042132421050033
73. Гомазков О.А. (2021) Поражение сосудистого эндотелия как ведущий механизм системной патологии COVID-19 // Успехи современной биологии. Т. 141. № 2. С. 118-127. DOI: 10.31857/S0042132421020058
74. Тарловская Е.И., Арутюнов А.Г., Конради А.О. и др. (2021) Анализ влияния препаратов базовой терапии, применявшихся для лечения сопутствующих заболеваний в период, предшествующий инфицированию, на риск летального исхода при новой коронавирусной инфекции. Данные международного регистра «Анализ динамики Коморбидных заболеваний у пациенТов, перенесшИх инфицироВание SARS-CoV-2» (AКТИВ SARS-CoV-2) // Кардиология. Т. 61. № 9. С. 20-32. DOI: 10.18087/cardio.2021.9.n1680
75. Сулимов А.В., Шихалиев Х.С., Пьянков О.В. и др. (2021) Разработка противовирусных лекарств на основе ингибиторов главной протеазы SARS-CoV-2 // Биомедицинская химия. Т. 67. № 3. С. 259-267. DOI: 10.18097/PBMC20216703259
76. Гайнитдинова В.В., Авдеев С.Н., Мержоева З.М. и др. (2021) Опыт применения N-ацетилцистеина в комплексном лечении среднетяжелой COVID-ассоциированной пневмонии // Пульмонология. Т. 31. С. 21-29. DOI: 10.18093/0869-0189-2021-31-1-21-29
77. Chia C.S.B., Xu W., Shuyi Ng. P. (2021) A Patent Review on SARS Coronavirus Main Protease (3CLpro) Inhibitors // ChemMedChem. V. 17. P. e202100576. DOI: 10.1002/cmdc.202100576
2022

1. Halford B. (2022) The path to Paxlovid. How Pfizer scientists transformed an old drug lead into an oral COVID-19 antiviral // ACS Cent. Sci. V. 8. No. 4. P. 405–407. DOI: 10.1021/acscentsci.2c00369
2. Ullrich S., Ekanayake K.B., Otting G., Nitsche C. (2022) Main protease mutants of SARS-CoV-2 variants remain susceptible to nirmatrelvir // Bioorg. Med. Chem. Lett. V. 62. P. 128629. DOI: 10.1016/j.bmcl.2022.128629
3. Patten J.J., Keiser P.T., Morselli-Gysi D. et al. (2022) Identification of potent inhibitors of SARS-CoV-2 infection by combined pharmacological evaluation and cellular network prioritization // iScience. V. 25. P. 104925. DOI: 10.1016/j.isci.2022.104925
4. Assmus F., Driouich J.S., Abdelnabi R. et al. (2022) Need for a Standardized Translational Drug Development Platform: Lessons Learned from the Repurposing of Drugs for COVID-19 // Microorganisms. V. 10. P. 1639. DOI: 10.3390/microorganisms10081639
5. Bai C., Zhong Q., Gao G.F. (2022) Overview of SARS-CoV-2 genome-encoded proteins // Sci. China Life Sci. V. 65. P. 280-294. DOI: 10.1007/s11427-021-1964-4
6. Hashimoto Y., Suzuki T., Hashimoto K. (2022) Mechanisms of action of fluvoxamine for COVID-19: a historical review // Mol Psychiatry. V. 27. P. 1898-1907. DOI: 10.1038/s41380-021-01432-3
7. Basu D., Chavda V.P., Mehta A.A. (2022) Therapeutics for COVID-19 and post COVID-19 complications: An update // Curr. Res. Pharmacol. Drug Discov. V. 3, P. 100086. DOI: 10.1016/j.crphar.2022.100086
8. Wagoner J., Herring S., Hsiang T.Y. et al. (2022) Combinations of host- and virus-targeting antiviral drugs confer synergistic suppression of SARS-CoV-2 // Microbiol. Spectr. V. 10. No. 5. P. e0333122. DOI: 10.1128/spectrum.03331-22
9. Wang X., Sacramento C.Q., Jockusch S. et al. (2022) Combination of antiviral drugs inhibits SARS-CoV-2 polymerase and exonuclease and demonstrates COVID-19 therapeutic potential in viral cell culture // Communications biology. V. 5. P. 154. DOI: 10.1038/s42003-022-03101-9
10. Chakraborty C., Sharma A.R., Bhattacharya M., Agoramoorthy G., Lee S.S. (2022) The Drug Repurposing for COVID-19 Clinical Trials Provide Very Effective Therapeutic Combinations: Lessons Learned From Major Clinical Studies // Front. Pharmacol. V. 12. P. 704205. DOI: 10.3389/fphar.2021.704205
11. Cho C.C., Li S.G., Lalonde T.J. et al. (2022) Drug Repurposing for the SARS-CoV-2 Papain-Like Protease // ChemMedChem. V. 17. P. e202100455. DOI: 10.1002/cmdc.202100455
12. Ledford H. (2022) Hundreds of COVID trials could provide a deluge of new drugs // Nature.V. 603. P. 25-27. DOI: 10.1038/d41586-022-00562-0
13. Hua Y., Dai X., Xu Y. et al. (2022) Drug repositioning: Progress and challenges in drug discovery for various diseases // Eur. J. Med. Chem. V. 234. P. 114239. DOI: 10.1016/j.ejmech.2022
14. Shytaj I,L,, Fares M,, Gallucci L. et al. (2022) Cobicistat Synergizes with Remdesivir To Inhibit SARS-CoV-2 Replication In Vitro and Decreases Viral Titers and Disease Progression in Syrian Hamsters // mBio. V. 13. P. e0370521. DOI: 10.1128/mbio.03705-21
15. Prieto Santamaría L., Díaz Uzquiano M., Ugarte Carro E. et al. (2022) Integrating heterogeneous data to facilitate COVID-19 drug repurposing // Drug Discov. Today. V. 27. P. 558-566. DOI: 10.1016/j.drudis.2021.10.002
16. Ngan D.K., Xu T., Xia M., Zheng W., Huang R. (2022) Repurposing drugs as COVID-19 therapies: A toxicity evaluation // Drug Discov. Today. V. 27. P. 1983-1993. DOI: 10.1016/j.drudis.2022.04.001
17. Chiu W., Verschueren L., Van den Eynde C. et al. (2022) Development and optimization of a high-throughput screening assay for in vitro anti-SARS-CoV-2 activity: Evaluation of 5676 Phase 1 Passed Structures // J. Med. Virol. V. 94. P. 3101-3111. DOI: 10.1002/jmv.27683
18. Jonsdottir H.R., Siegrist D., Julien T. et al. (2022) Molnupiravir combined with different repurposed drugs further inhibits SARS-CoV-2 infection in human nasal epithelium in vitro // Biomed. Pharmacother. V. 150. P. 113058. DOI: 10.1016/j.biopha.2022.113058
19. Yip A.J.W., Low Z.Y., Chow V.T.K., Lal S.K. (2022) Repurposing Molnupiravir for COVID-19: The Mechanisms of Antiviral Activity // Viruses. V. 14. P. 1345. DOI: 10.3390/v14061345
20. Robinson B.W.S., Tai A., Springer K. (2022) Why we still need drugs for COVID-19 and can't just rely on vaccines // Respirology. V. 27. P. 109-111. DOI: 10.1038/10.1111/resp.14199
21. Ferraresi A., Isidoro C. (2022) Will Omics Biotechnologies Save Us from Future Pandemics? Lessons from COVID-19 for Vaccinomics and Adversomics // Biomedicines. V. 11. P. 52. DOI: 10.3390/biomedicines11010052
22. Shcherbakov D., Baev D., Kalinin M. et al. (2022) Design and Evaluation of Bispidine-Based SARS-CoV-2 Main Protease Inhibitors // ACS Med. Chem. Lett. V. 13. No. 1. P. 140–147. DOI: 10.1021/acsmedchemlett.1c00299
23. Narayanan A., Narwal M., Majowicz S.A. et al. (2022) Identification of SARS-CoV-2 inhibitors targeting Mpro and PLpro using in-cell-protease assay // Commun. Biol. V. 5. P. 169. DOI: 10.1038/s42003-022-03090-9
24. Chupakhin O.N., Rusinov V..L, Varaksin M.V. et al. (2022) Triazavirin-A Novel Effective Antiviral Drug // Int. J. Mol. Sci. V. 23. P. 14537. DOI: 10.3390/ijms232314537
25. Kostyusheva A., Brezgin S., Babin Y. et al. (2022) CRISPR-Cas systems for diagnosing infectious diseases // Methods. V. 203. P. 431-446. DOI: 10.1016/j.ymeth.2021.04.007
26. Nersisyan S., Zhiyanov A., Shkurnikov M., Tonevitsky A. (2022) T-CoV: a comprehensive portal of HLA-peptide interactions affected by SARS-CoV-2 mutations // Nucleic Acids Res. V. 50(D1). P. D883-D887. DOI: 10.1093/nar/gkab701
27. Bagrov D.V., Glukhov G.S., Moiseenko A.V. et al. (2022) Structural characterization of β-propiolactone inactivated severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) particles // Microsc Res Tech. V. 85. P. 562-569. DOI: 10.1002/jemt.23931
28. Kolpakov F., Akberdin I., Kiselev I. et al. (2022) BioUML-towards a universal research platform // Nucleic Acids Res. V. 50(W1). P. W124–31. DOI: 10.1093/nar/gkac286
29. Puhl A.C., Gomes G.F., Damasceno S. et al. (2022) Pyronaridine Protects against SARS-CoV-2 Infection in Mouse // ACS Infect Dis. V. 8. P. 1147-1160. DOI: 10.1021/acsinfecdis.2c00091
30. Shkoda A.S., Gushchin V..A, Ogarkova D.A. et al. (2022) Sputnik V Effectiveness against Hospitalization with COVID-19 during Omicron Dominance // Vaccines (Basel). V. 10. P. 938. DOI: 10.3390/vaccines10060938
31. Fomenko V.V., Rudometova N.B., Yarovaya O.I. et al. (2022) Synthesis and In Vitro Study of Antiviral Activity of Glycyrrhizin Nicotinate Derivatives against HIV-1 Pseudoviruses and SARS-CoV-2 Viruses // Molecules. V. 27. P. 295. DOI: 10.3390/molecules27010295
32. Makarov V.A., Popov V.O. (2022) PDSTP Is the First Drug in Class to Treat Coronavirus Infection // Her. Russ. Acad. Sci. V. 92. P. 488-490. DOI: 10.1134/S1019331622040190
33. Ivashchenko A.A., Zagribelnyy B.A., Ivanenkov Y.A. et al. (2022) The Efficacy of Aprotinin Combinations with Selected Antiviral Drugs in Mouse Models of Influenza Pneumonia and Coronavirus Infection Caused by SARS-CoV-2 // Molecules. V. 27. P. 4975. DOI: 10.3390/molecules27154975
34. Гомазков О.А. (2022) Нейропилин – новый игрок в патогенезе COVID-19 // Нейрохимия. Т. 39. № 2. С. 124-130. DOI: 10.31857/S1027813322020066
35. Гомазков О.А. (2022) Нейротропизм как механизм поражающего действия коронавируса // Успехи современной биологии. Т. 142. № 4. С. 406-416. DOI: 10.31857/S0042132422040068
36. Иванова Я.О., Воронина А.И., Скворцов В.С. (2022) Предсказание ингибирования главной протеазы SARS-CoV-2 c учётом фильтрации данных о положении лигандов // Биомедицинская химия. Т. 68. № 6. С. 444-458. DOI: 10.18097/PBMC20226806444
37. Oh C.K., Nakamura T., Beutler N. et al. (2023) Targeted protein S-nitrosylation of ACE2 inhibits SARS-CoV-2 infection // Nature chemical biology. V. 19. P. 275-283. DOI: 10.1038/s41589-022-01149-6
38. Silva V., Radic M. (2022) COVID-19 Pathology Sheds Further Light on Balance between Neutrophil Proteases and Their Inhibitors // Biomolecules. V. 13. P. 82. DOI: 10.3390/biom13010082
39. Zhang Y., Juhas M., Kwok C.K. (2022) Aptamers targeting SARS-COV-2: a promising tool to fight against COVID-19 // Trends Biotechnol. V. 41. P. 528-544. DOI: 10.1016/j.tibtech.2022.07.012
40. Lundstrom K., Hromić-Jahjefendić A., Bilajac E. et al. (2022) COVID-19 signalome: Pathways for SARS-CoV-2 infection and impact on COVID-19 associated comorbidity // Cell Signal. V. 101. P. 110495. DOI: 10.1016/j.cellsig.2022.110495
41. Ng W.H., Tang P.C.H., Mahalingam S., Liu X. (2023) Repurposing of drugs targeting the cytokine storm induced by SARS-CoV-2 // Br. J. Pharmacol. V. 180. P. 133-143. DOI: 10.1111/bph.15987
42. Jahirul Islam M., Nawal Islam N., Siddik Alom M. et al. (2022) A review on structural, non-structural, and accessory proteins of SARS-CoV-2: Highlighting drug target sites // Immunobiology. V. 228. P. 152302. DOI: 10.1016/j.imbio.2022.152302
43. Lim S.P. (2022) Targeting SARS-CoV-2 and host cell receptor interactions // Antiviral Res. V. 210. P. 105514. DOI: 10.1016/j.antiviral.2022.105514
44. Bilezikian J.P., Binkley N., De Luca H.F. (2023) Consensus and controversial aspects of vitamin D and COVID-19 // The Journal of Clinical Endocrinology & Metabolism. V. 108. P. 1034-1042. DOI: 10.1210/clinem/dgac719
44. Bilezikian J.P., Binkley N., De Luca H.F. (2023) Consensus and controversial aspects of vitamin D and COVID-19 // The Journal of Clinical Endocrinology & Metabolism. V. 108. P. 1034-1042. DOI: 10.1210/clinem/dgac719
2023

1. Saravolatz L.D., Depcinski S., Sharma M. (2023) Molnupiravir and Nirmatrelvir-Ritonavir: Oral Coronavirus Disease 2019 Antiviral Drugs // Clin. Infect. Dis. V. 76. P. 165-171. DOI: 10.1093/cid/ciac180
2. Zheng Q., Ma P., Wang M. et al. (2023) Efficacy and safety of Paxlovid for COVID-19:a meta-analysis // J. Infect. V. 86, P. 66-117. DOI: 10.1016/j.jinf.2022.09.027
3. Murakami N., Hayden R., Hills T. et al. (2023) Therapeutic advances in COVID-19 // Nat. Rev. Nephrol. V. 19. P. 38-52. DOI: 10.1038/s41581-022-00642-4
4. Msemburi W., Karlinsky A., Knutson V.et al. (2023) The WHO estimates of excess mortality associated with the COVID-19 pandemic // Nature. V. 613. P. 130-137. DOI: 10.1038/s41586-022-05522-2
5. Pilla Reddy V., El-Khateeb E., Jo H. et al. (2023) Pharmacokinetics under the COVID-19 storm // Br. J. Clin. Pharmacol. V. 89. P. 158-186. DOI: 10.1111/bcp.14668
6. Rannard S.P., McDonald T.O., Owen A. (2023) Chasing COVID-19 chemotherapeutics without putting the cart before the horse // Br. J. Clin. Pharmacol. V. 89. P. 421-423. DOI: 10.1111/bcp.14575
7. Su J., Shen S., Hu Y. et al. (2023) SARS-CoV-2 ORF3a inhibits cGAS-STING-mediated autophagy flux and antiviral function // J. Med. Virol. V. 95. P. e28175. DOI: 10.1002/jmv.28175
8. Pérez-Vargas J., Shapira T., Olmstead A.D. et al. (2023) Discovery of lead natural products for developing pan-SARS-CoV-2 therapeutics // Antiviral research. V. 209. Article ID: 105484. DOI: 10.1016/j.antiviral.2022.105484
9. Davis H.E., McCorkell L., Vogel J.M., Topol E.J. (2023) Long COVID: major findings, mechanisms and recommendations // Nat. Rev. Microbiol. V. 21. P. 133-146 DOI: 10.1038/s41579-022-00846-2
10. Jahirul Islam M., Nawal Islam N., Siddik Alom M., Kabir M., Halim M.A. (2023) A review on structural, non-structural, and accessory proteins of SARS-CoV-2: Highlighting drug target sites // Immunobiology. V. 228. P. 152302. DOI: 10.1016/j.imbio.2022.152302
11. Boytz R., Słabicki M., Ramaswamy S. et al. (2023) Anti-SARS-CoV-2 activity of targeted kinase inhibitors: Repurposing clinically available drugs for COVID-19 therapy // J. Med. Virol. V. 95. P. e28157. DOI: 10.1002/jmv.28157
12. Frigerio R., Musicò A., Strada A. et al. (2023) Epitope Mapping on Microarrays Highlights a Sequence on the N Protein with Strong Immune Response in SARS-CoV-2 Patients // Methods Mol Biol. V. 2578. P. 209-217. DOI: 10.1007/978-1-0716-2732-7_15
13. Liu X., Hasan M.R., Ahmed .KA., Hossain M.Z. (2023) Machine learning to analyse omic-data for COVID-19 diagnosis and prognosis // BMC Bioinformatics. V. 24. P.7. DOI: 10.1186/s12859-022-05127-6
14. Sui L., Li L., Zhao Y. et al. (2023) Host cell cycle checkpoint as antiviral target for SARS-CoV-2 revealed by integrative transcriptome and proteome analyses // Signal Transduct. Target. Ther. V. 8. P. 21. DOI: 10.1038/s41392-022-01296-1
15. Pérez-Vargas J., Shapira T., Olmstead A.D. et al. (2023) Discovery of lead natural products for developing pan-SARS-CoV-2 therapeutics // Antiviral research. V. 209. Article ID: 105484. DOI: 10.1016/j.antiviral.2022.105484
16. Smith E., Davis-Gardner M.E., Garcia-Ordonez R.D. et al. (2023) High throughput screening for drugs that inhibit 3C-like protease in SARS-CoV-2 // SLAS Discov. V. 28. P. 95-101. DOI: 10.1016/j.slasd.2023.01.001
17. Omenn G.S., Lane L., Overall C.M. et al. (2023) The 2023 Report on the Proteome from the HUPO Human Proteome Project // J. Proteome Res. DOI: 10.1021/acs.jproteome.3c00591
18. Brindani N., Munafò F., Menichetti A. et al. (2023) Design, synthesis, docking, and biochemical characterization of non-nucleoside SARS-CoV-2 RdRp inhibitors // Bioorg. Med. Chem. V. 80. P. 117179. DOI: 10.1016/j.bmc.2023.117179
19. Vuorio A., Raal F., Kovanen P.T. (2023) Drug-drug interaction with oral antivirals for the early treatment of COVID-19 // Int. J. Infect. Dis. V. 127. P. 171-172. DOI: 10.1016/j.ijid.2022.11.039
20. Collins F., Adam S., Colvis C. et al. (2023) The NIH-led research response to COVID-19 // Science. V. 379. P. 441-444. DOI: 10.1126/science.adf5167
21. Joshi R.P., Schultz K.J., Wilson J.W. et al. (2023) AI-Accelerated Design of Targeted Covalent Inhibitors for SARS-CoV-2 // J. Chem. Inf. Model. V. 63. P. 1438-1453. DOI: 10.1021/acs.jcim.2c01377
22. Wamser R., Pach S., Arkona C. et al. (2023) A Critical Study on Acylating and Covalent Reversible Fragment Inhibitors of SARS-CoV-2 Main Protease Targeting the S1 Site with Pyridine // ChemMedChem. V. 22. Article ID: e202200635. DOI: 10.1002/cmdc.202200635
23. Gentile F., Oprea T.I,, Tropsha A., Cherkasov A. (2023) Surely you are joking, Mr Docking! // Chem. Soc Rev. Epub ahead of print. DOI: 10.1039/d2cs00948j
24. Davis H.E., McCorkell L., Vogel J.M., Topol E.J. (2023) Long COVID: major findings, mechanisms and recommendations // Nat. Rev. Microbiol. V. 13. P. 1–14. DOI: 10.1038/s41579-022-00846-2
25. Prasetiya F.S., Destiarani W., Nuwarda R.F. et al. (2023) The nanomolar affinity of C-phycocyanin from virtual screening of microalgal bioactive as potential ACE2 inhibitor for COVID-19 therapy // J. King. Saud. Univ. Sci. V. 35. P. 102533. DOI: 10.1016/j.jksus.2022.102533
26. Malone B.F., Perry J.K., Olinares P.D.B. et al. (2023) Structural basis for substrate selection by the SARS-CoV-2 replicase // Nature. V. 614. P. 781–787. DOI: 10.1038/s41586-022-05664-3
27. Panahi Y., Gorabi A.M., Talaei S. et al. (2023) An overview on the treatments and prevention against COVID-19 // Virology Journal. V. 20. P. 1-29. DOI: 10.1186/s12985-023-01973-9
28. Khan A.M., Atia-Tul-Wahab, Farooq S. et al. (2023) Repurposing of US-FDA approved drugs against SARS-CoV-2 main protease (Mpro) by using STD-NMR spectroscopy, in silico studies and antiviral assays // Int. J. Biol. Macromol. V. 234. P. 123540. DOI: 10.1016/j.ijbiomac.2023.123540
29. Russell C.D., Lone N.I., Baillie J.K. (2023) Comorbidities, multimorbidity and COVID-19 // Nature medicine. V. 29. P. 334-343. DOI: 10.1038/s41591-022-02156-9
30. Chaguza C., Hahn A.M., Petrone M.E. et al. (2023) Accelerated SARS-CoV-2 intrahost evolution leading to distinct genotypes during chronic infection // Cell Reports Medicine V. 4. Article ID: 100943. DOI: 10.1016/j.xcrm.2023.100943
31. Wang X., Wang H., Yin G. et al. (2023) Network-based drug repurposing for the treatment of COVID-19 patients in different clinical stages // Heliyon. V. 9. P. e14059. DOI: 10.1016/j.heliyon.2023.e14059
32. Lundstrom K., Hromić-Jahjefendić A., Bilajac E. et al. (2023) COVID-19 signalome: Potential therapeutic interventions // Cell Signal. V. 103. Article ID: 110559. DOI: 10.1016/j.cellsig.2022.110559
33. Chatterjee S., Nalla L.V., Sharma M et al. (2023) Association of COVID-19 with Comorbidities: An Update // ACS Pharmacol. Transl. Sci. V. 6. P. 334-354. DOI: 10.1021/acsptsci.2c00181
34. Pozzi C., Vanet A., Francesconi V. et al. (2023) Anti-SARS-CoV-2 Leads, Drugs, and the Drug Discovery-Genetics Alliance Perspective // J. Med. Chem. V. 66. P. 3664-3702. DOI: 10.1021/acs.jmedchem.2c01229
35. Kovacic S., Ng K., Pandey M. et al. (2023) A. Large-Scale Virtual Screening for the Discovery of SARS-CoV-2 Papain-like Protease (PLpro) Non-covalent Inhibitors // J. Chem. Inf. Model. V. 63. P. 2158-2169. DOI: 10.1021/acs.jcim.2c01641
36. Wang R., Lee J.H., Kim J. et al. (2023) SARS-CoV-2 restructures host chromatin architecture // Nat. Microbiol. V. 8. P. 679-694. DOI: 10.1038/s41564-023-01344-8
37. Bekheit M.S., Panda S.S., Girgis A.S. (2023) Potential RNA-dependent RNA polymerase (RdRp) inhibitors as prospective drug candidates for SARS-CoV-2 // Eur. J. Med. Chem. V. 252. P. 115292. DOI: 10.1016/j.ejmech.2023.115292
38. Hernán M.A., Del Amo J. (2023) Drug Repurposing and Observational Studies: The Case of Antivirals for the Treatment of COVID-19 // Ann. Intern. Med. V. 176. P. 556-560. DOI: 10.7326/M22-3582
39. Avdonin P.P., Rybakova E.Y., Trufanov S.K. et al. (2023) SARS-CoV-2 Receptors and Their Involvement in Cell Infection // Biochem. Moscow Suppl. Ser. A. V. 17. P. 1–11. DOI: 10.1134/S1990747822060034
40. Stefanelli I., Corona A., Cerchia C. et al. (2023) Broad-spectrum coronavirus 3C-like protease peptidomimetic inhibitors effectively block SARS-CoV-2 replication in cells: Design, synthesis, biological evaluation, and X-ray structure determination // Eur. J. Med. Chem. V. 253. P. 115311. DOI: 10.1016/j.ejmech.2023.115311
41. Votto M., Castagnoli R., Marseglia G.L. et al. (2023) COVID-19 and autoimmune diseases: is there a connection? // Current Opinion in Allergy and Clinical Immunology. V. 23. P. 185-192. DOI: 10.1097/ACI.0000000000000888
42. Shin Y.S., Lee J.Y., Jeon S. et al. (2023) Discovery of 2-aminoquinolone acid derivatives as potent inhibitors of SARS-CoV-2 // Bioorg. Med. Chem. Lett. V.85. P. 129214. DOI: 10.1016/j.bmcl.2023.129214
43. Smith E., Davis-Gardner M.E., Garcia-Ordonez R.D. et al. (2023) High Throughput Screening for Drugs that Inhibit 3C-Like Protease in SARS-CoV-2 // SLAS Discov. V. 13. P. S2472-5552(23)00001-1. DOI: 10.1016/j.slasd.2023.01.001
44. Kronenberger T., Laufer S.A., Pillaiyar T. (2023) COVID-19 therapeutics: Small-molecule drug development targeting SARS-CoV-2 main protease // Drug Discov. Today. V. 28. P. 103579. DOI: 10.1016/j.drudis.2023.103579. DOI: 10.1016/j.drudis.2023.103579
45. Markov P.V., Ghafari M., Beer M. et al (2023) The evolution of SARS-CoV-2 // Nat. Rev. Microbiol. V. 21. P. 361-379. DOI: 10.1038/s41579-023-00878-2
46. Ghorbanali Z., Zare-Mirakabad F., Akbari M. et al. (2023) DrugRep-KG: Toward Learning a Unified Latent Space for Drug Repurposing Using Knowledge Graphs // J. Chem. Inf. Model. V. 63. P. 2532-2545. DOI: 10.1021/acs.jcim.2c01291
47. Kumar S., Basu M., Ghosh P. et al. (2023) COVID-19 therapeutics: Clinical application of repurposed drugs and futuristic strategies for target-based drug discovery // Genes Dis. V. 10. P. 1402-1428. DOI: 10.1016/j.gendis.2022.12.019
48. Hersi F., Sebastian A., Tarazi H. et al. (2023) Discovery of novel papain-like protease inhibitors for potential treatment of COVID-19 // Eur. J. Med. Chem. V. 254. P. 115380. DOI: 10.1016/j.ejmech.2023.115380
49. Li G., Hilgenfeld R., Whitley R. et al. (2023) Therapeutic strategies for COVID-19: progress and lessons learned // Nat. Rev. Drug Discov. V. 22. P. 449–475. DOI: 10.1038/s41573-023-00672-y
50. Vaz E.S., Vassiliades S.V., Giarolla J. et al. (2023) Drug repositioning in the COVID-19 pandemic: fundamentals, synthetic routes, and overview of clinical studies // Eur. J. Clin. Pharmacol. V. 79. P. 723-751. DOI: 10.1007/s00228-023-03486-4
51. Su Y., Wu J., Li X. et al. (2023) DTSEA: A network-based drug target set enrichment analysis method for drug repurposing against COVID-19 // Comput. Biol. Med. V. 159. P. 106969. DOI: 10.1016/j.compbiomed.2023.106969
52. von Delft A., Hall M.D., Kwong A.D. et al. (2023) Accelerating antiviral drug discovery: lessons from COVID-19 // Nat. Rev. Drug Discov. V. 22. P. 585–603. DOI: 10.1038/s41573-023-00692-8
53. Pang X., Xu W., Liu Y. et al. (2023) The research progress of SARS-CoV-2 main protease inhibitors from 2020 to 2022 // Eur. J. Med. Chem. V. 257. P. 115491. DOI: 10.1016/j.ejmech.2023.115491
54. Mehyar N. (2023) Coronaviruses SARS-CoV, MERS-CoV, and SARS-CoV-2 helicase inhibitors: a systematic review of invitro studies // J. Virus Erad. V. 9. P. 100327. DOI: 10.1016/j.jve.2023.100327
55. Ahmed M.S., Farag A.B., Boys I.N. (2023) FDA approved drugs with antiviral activity against SARS-CoV-2: From structure-based repurposing to host-specific mechanisms // Biomed. Pharmacother. V. 162. Article ID: 114614. DOI: 10.1016/j.biopha.2023.114614
56. Augustin Y., Staines H.M., Velavan T.P. et al. (2023) Drug repurposing for COVID-19: current evidence from randomized controlled adaptive platform trials and living systematic reviews // Br. Med. Bull. V. 147. P. 31-49. DOI: 10.1093/bmb/ldac037
57. Brian Chia C.S., Pheng Lim S. (2023) A Patent Review on SARS Coronavirus Papain-Like Protease (PLpro) Inhibitors // ChemMedChem. V. 18. P. e202300216. DOI: 10.1002/cmdc.202300216
58. Peterson A.A., Liu D.R. (2023) Small-molecule discovery through DNA-encoded libraries // Nat. Rev. Drug Discov. V. 22. P. 699–722. DOI: 10.1038/s41573-023-00713-6
59. Sebők S., Gyires K. (2023) Long COVID and possible preventive options // Inflammopharmacol. V. 31. P. 2807–2817. DOI: 10.1007/s10787-023-01204-1
60. Viskupicova J., Rezbarikova P., Kovacikova L. et al. (2023) Inhibitors of SARS-CoV-2 main protease: Biological efficacy and toxicity aspects // Toxicol. In Vitro. V. 92. P. 105640. DOI: 10.1016/j.tiv.2023.105640
61. Brett J., Bahceci D., Lipworth W. et al. (2023) Can old drugs learn new tricks? Achieving registration and public subsidy listing for off-patent medicines with novel therapeutic applications // Intern. Med. J. V. 53. P. 1284-1287. DOI: 10.1111/imj.16159
62. Dinda B., Dinda M., Dinda S. et al. (2023) An overview of anti-SARS-CoV-2 and anti-inflammatory potential of baicalein and its metabolite baicalin: Insights into molecular mechanisms // Eur. J. Med. Chem. V. 258. P. 115629. DOI: 10.1016/j.ejmech.2023.115629
63. Yao Y., Zhang Y., Li Z. et al. (2023) A deep learning-based drug repurposing screening and validation for anti-SARS-CoV-2 compounds by targeting the cell entry mechanism // Biochem. Biophys. Res. Commun. V. 675. P. 113-121. DOI: 10.1016/j.bbrc.2023.07.018
64. Tan B., Sacco M., Tan H. et al. (2023) Exploring diverse reactive warheads for the design of SARS-CoV-2 main protease inhibitors // Eur. J. Med. Chem. V. 259. P. 115667. DOI: 10.1016/j.ejmech.2023.115667
65. Puhl A.C., Lane T.R., Ekins S. (2023) Learning from COVID-19: How drug hunters can prepare for the next pandemic // Drug Discov. Today. V. 28. P. 103723. DOI: 10.1016/j.drudis.2023.103723
66. Xu L., Chen R., Liu J. et al. (2023) Analyzing 3D structures of the SARS-CoV-2 main protease reveals structural features of ligand binding for COVID-19 drug discovery // Drug Discov. Today. V. 28. P. 103727. DOI: 10.1016/j.drudis.2023.103727
67. Elkashlan M., Ahmad R.M., Hajar M. et al. (2023) A review of SARS-CoV-2 drug repurposing: databases and machine learning models // Front. Pharmacol. V. 14. Article ID: 1182465. DOI: 10.3389/fphar.2023.1182465
68. Zhang F., Luna A., Tan T. et al. (2023) COVIDpro: Database for Mining Protein Dysregulation in Patients with COVID-19 // J. Proteome Res. V. 22. P. 2847-2859. DOI: 10.1021/acs.jproteome.3c00092
69. Kushwaha N.D., Mohan J., Kushwaha B. et al. (2023) A comprehensive review on the global efforts on vaccines and repurposed drugs for combating COVID-19 // Eur. J. Med. Chem. V. 260. P. 115719. DOI: 10.1016/j.ejmech.2023.115719
70. Pitsillou E., Beh R.C., Liang J.J. et al. (2023) EpiMed Coronabank Chemical Collection: Compound selection, ADMET analysis, and utilisation in the context of potential SARS-CoV-2 antivirals // J. Mol. Graph. Model. V. 125. P. 108602. DOI: 10.1016/j.jmgm.2023.108602
71. Valipour M., Irannejad H., Keyvani H. (2023) An Overview on Anti-COVID-19 Drug Achievements and Challenges Ahead // ACS Pharmacol. Transl. Sci. V. 6. P. 1248-1265. DOI: 10.1021/acsptsci.3c00121
72. Zhang F.M., Huang T., Wang F. et al. (2023) Discovery of highly potent covalent SARS-CoV-2 3CLpro inhibitors bearing 2-sulfoxyl-1,3,4-oxadiazole scaffold for combating COVID-19 // Eur. J. Med. Chem. V. 260. P. 115721. DOI: 10.1016/j.ejmech.2023.115721
73. Martin H.J., Melo-Filho C.C., Korn D. et al. (2023) A. Small molecule antiviral compound collection (SMACC): A comprehensive, highly curated database to support the discovery of broad-spectrum antiviral drug molecules // Antiviral Res. V.217. Article ID: 105620. DOI: 10.1016/j.antiviral.2023.105620
74. Boytz R., Słabicki M., Ramaswamy S. et al. (2023) Anti‐SARS‐CoV‐2 activity of targeted kinase inhibitors: repurposing clinically available drugs for COVID‐19 therapy // Journal of medical virology. V. 95. Article ID: e28157. DOI: 10.1002/jmv.28157
75. Wilks S.H., Mühlemann B., Shen X. et al. (2023) Mapping SARS-CoV-2 antigenic relationships and serological responses // Science. V. 382. Article ID: eadj0070. DOI: 10.1126/science.adj0070
76. Zhou Y., Liu Y., Gupta S. et al. (2023) A comprehensive SARS-CoV-2–human protein–protein interactome reveals COVID-19 pathobiology and potential host therapeutic targets // Nature biotechnology. V. 41. P. 128-139. DOI: 10.1038/s41587-022-01474-0
77. Kim D.K., Weller B., Lin C.W. et al. (2023) A proteome-scale map of the SARS-CoV-2–human contactome // Nature Biotechnology. V. 41. P. 140-149. DOI: 10.1038/s41587-022-01475-z
78. Schimunek J., Seidl P., Elez K. et al. (2023) A community effort in SARS-CoV-2 drug discovery // Molecular Informatics, 2023 Oct 13. Article ID: e202300262. DOI: 10.1002/minf.202300262
79. Zhang Y., Li Y. (2023) Clinical Translation of Aptamers for COVID-19 // J. Med. Chem. V. 66. P. 16568–16578. DOI: 10.1021/acs.jmedchem.3c01607
80. Chen J., Zhou Y., Wei X. et al. (2023) Development of Pan-Anti-SARS-CoV-2 Agents through Allosteric Inhibition of nsp14/nsp10 Complex // ACS Infect. Dis. DOI: 10.1021/acsinfecdis.3c00356
81. Iketani S., Mohri H., Culbertson B. et al. (2023) Multiple pathways for SARS-CoV-2 resistance to nirmatrelvir // Nature. V. 613. P. 558-564. DOI: 10.1038/s41586-022-05514-2
82. Sang X., Wang J., Zhou J. et al. (2023) A Chemical Strategy for the Degradation of the Main Protease of SARS-CoV-2 in Cells // J. Am. Chem. Soc. V. 145. P. 27248–27253. DOI: 10.1021/jacs.3c12678
83. Tropsha A., Isayev O., Varnek A. et al. (2023) Integrating QSAR modelling and deep learning in drug discovery: the emergence of deep QSAR // Nat. Rev. Drug Discov. DOI: 10.1038/s41573-023-00832-0
84. Oktavianawati I., Santoso M., Bakar M.F.A. et al. (2023) Recent progress on drugs discovery study for treatment of COVID-19: repurposing existing drugs and current natural bioactive molecules // Appl. Biol. Chem. V. 66. P. 89. DOI: 10.1186/s13765-023-00842-x
85. Teng O., Quek A.M.L., Nguyen T.M. et al. (2023) Biomarkers of early SARS-CoV-2 infection before the onset of respiratory symptoms // Clin. Microbiol. Infect. DOI: 10.1016/j.cmi.2023.12.024
2024

1. Agyarko R., Al Slail F., Garrett D.O. et al. (2024) The imperative for global cooperation to prevent and control pandemics // In: Modernizing Global Health Security to Prevent, Detect, and Respond. Academic Press. P. 53-69. Paperback ISBN: 9780323909457 / eBook ISBN: 9780323909464
2. Wu A., Shi K., Wang J. et al. (2024) Targeting SARS-CoV-2 entry processes: The promising potential and future of host-targeted small-molecule inhibitors // Eur. J. Med. Chem. V. 263. Article ID: 115923. DOI: 10.1016/j.ejmech.2023.115923
3. Pradelle A., Mainbourg S., Provencher S. et al. (2024) Deaths induced by compassionate use of hydroxychloroquine during the first COVID-19 wave: an estimate // Biomed. Pharmacother. V. 171. Article ID: 116055. DOI: 10.1016/j.biopha.2023.116055
4. Marrone G., Covino M., Merra G. et al. (2024) Ursodeoxycholic acid does not affect the clinical outcome of SARS-CoV-2 infection: A retrospective study of propensity score-matched cohorts // Liver Int. V. 44. P. 83-92. DOI: 10.1111/liv.15736
5. Nandi S., Kumar M., Saxena A.K. (2024) QSAR of SARS-CoV-2 main protease inhibitors utilizing theoretical molecular descriptors // Letters in Drug Design & Discovery. V. 21. P. 116-132. DOI: 10.2174/1570180820666221214151614
6. Zanini G., Selleri V., Roncati L. et al. (2024) Vascular “long COVID”: a new vessel disease? // Angiology. V. 75. P. 8-14. DOI: 10.1177/00033197231153204
7. Boccellino M. (2024) COVID-19 pandemic: therapeutic strategies and vaccines // Int. J. Mol. Sci. V. 25. Article ID: 556. DOI: 10.3390/ijms25010556
8. Bogacheva M.S., Kuivanen S., Potdar S. et al. (2024) Drug repurposing platform for deciphering the druggable SARS-CoV-2 interactome // Antiviral Res.. DOI: 10.1016/j.antiviral.2024.105813
9. Zhang D., Kukkar D., Kim K.H. et al. (2024) A comprehensive review on immunogen and immune-response proteins of SARS-CoV-2 and their applications in prevention, diagnosis, and treatment of COVID-19 // Int. J. Biol. Macromol. V. 259. P. 129284. DOI: 10.1016/j.ijbiomac.2024.129284

Ингибирование главной протеазы 3CLpro коронавируса SARS-CoV-2

Compositions and methods for inhibition of SARS-CoV-2 viral infections
2021.11.25 WO 2021/236134 A1
Настоящее изобретение предоставляет методы лечения COVID-19 путем введения фармацевтической композиции, обеспечивающей ингибирование основной протеазы (MPro) SARS-CoV-2 у пациента. Кроме того, настоящее изобретение предоставляет композиции и методы, которые могут быть направлены на ингибирование цитопатогенного эффекта (CPE), индуцированного вирусом SARS-CoV-2. В некоторых аспектах фармацевтическая композиция включает соединение, выбранное из группы, состоящей из пимозида (pimozide), эбастина (ebastine) и бепридила (bepridil), с лучшими значениями IC50 для ингибирования MPro. В целом, результаты, описанные в настоящем документе, показывают, что бепридил наиболее эффективен как в предотвращении проникновения SARS-CoV-2 в клетки-хозяева млекопитающих, так и в предотвращении репликации SARS-CoV-2 в клетках-хозяевах млекопитающих.
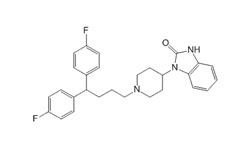
Пимозид — антипсихотическое средство класса дифенилбутилпиперидинов.
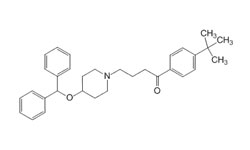
Эбастин — блокатор H1-гистаминовых рецепторов длительного действия второго поколения.
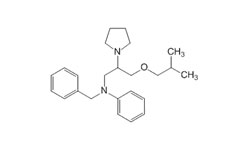
Бепридил — блокатор диаминовых кальциевых каналов, со значительной антиангинальной активностью
Use Of Tafenoquine, Boceprevir Or Narlaprevir For Treating Infection Of SARS-COV-2 And Medical Composition Thereof
2021.10.28 US 2021/330661 A1
Раскрывается метод ингибирования активности основной протеазы (Mpro) SARS-CoV-2, включающий контактирование с достаточной концентрацией тафенохина (Tafenoquine), боцепревира (Boceprevir) или нарлапревира (Narlaprevir). Тафенохин, боцепревир и нарлапревир способны подавлять активность основной протеазы SARS-CoV-2, а затем предотвращать или подавлять синтез вирусной РНК SARS-CoV-2 в клетках, поэтому они могут быть использованы для производства медицинской композиции для применения в лечении инфекции SARS-CoV-2. Метод ингибирования активности основной протеазы (M pro ) SARS- CoV- 2 включает контактирование SARS-CoV-2 с достаточной концентрацией тафенохина от 30 мкМ до 500 мкМ; для боцепревира IC50= 15,2±3,3 мкМ, для нарлапревира IC50= 40,8±4,6 мкМ.
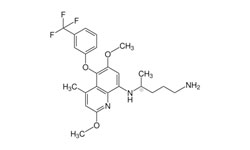
Тафенохин — лекарственный препарат для профилактики и лечения малярии.
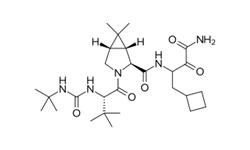
Боцепревир — ингибитор протеазы, используемый для лечения гепатита, вызванного вирусом гепатита С генотипа 1.
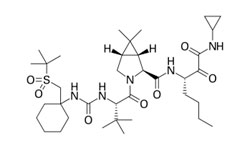
Нарлапревир - противовирусное средство, ингибитор NS3 сериновой протеазы вируса гепатита С.
SARS-CoV-2 inactivation by Ethacridine
2022.05.05 WO 2022093871 Al
Настоящее изобретение касается разработки новой скрининговой платформы для выявления ингибиторов Mpro. Объем изобретения охватывает композиции и соответствующие способы их применения для идентификации новых ингибиторов вирусных протеаз, таких как Mpro. Раскрывается фармацевтическая композиция, включающая этакридин (Ethacridine) или его производные, для использования в методе лечения вирусной инфекции у субъекта, в частности, SARS-CoV-2. Этакридин продемонстрировал значительную противовирусную активность (EC50 ~ 0,08 мкМ, IC50 ~ 3,54 мкМ).
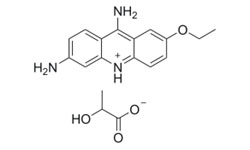
Этакридин - это ароматическое производное акридина, обладающее антисептическими и абортивными свойствами.
Application of Gossypol and derivatives and analogues thereof in preparation of anti novel coronavirus and similar RNA virus products
2022.12.22 WO 2022261852 A1
Изобретение раскрывает применение госсипола (Gossypol), природного продукта, получаемого из хлопка, и его производных в приготовлении лекарств против нового коронавируса и подобных РНК-вирусов. Исследователи установили, что госсипол и его производные могут ингибировать комбинацию папаиноподобной протеазы (NSP3, PLpro), основной протеазы (NSP5, Mpro), РНК-зависимой РНК-полимеразы (NSP12, RdRp), хеликазы (NSP13, helicase), экзонуклеазы (NSP14, 3'-to-5'экзонуклеаза), эндонуклеазы (NSP15, эндоРНКза), метилтрансферазы (NSP16, 2'-O-рибоза метилтрансфераза) и других белков, тем самым эффективно подавляя репликацию нового коронавируса и подобных ему РНК-вирусов in vitro и in vivo. При ингибировании Mpro IC50 находится в пределах 1,59 мкМ-1,74 мкМ, EC50=0,21 мкМ.
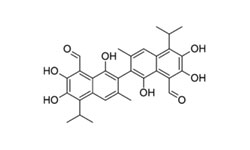
Госсипол — природный полифенол, жёлтый пигмент, получаемый из хлопчатника, ингибитор ряда ферментов-дегидрогеназ; подавляет сперматогенез и испытывался в Китае в качестве орального контрацептива для мужчин.
Medicine for preventing or treating novel coronavirus infection
2023.07.25 CN 116474072 A
Изобретение раскрывает применение гозерелина, хинеприна, идарубицина и/или ретапамулина для профилактики или лечения новой коронавирусной инфекции. Лекарственное средство дополнительно содержит производные гозерелина, хинеприна, идарубицина и/или ретапамулина или композицию, содержащую лекарственное средство. Основная протеаза нового коронавируса (протеаза 3CL) может участвовать в разрезании полипротеина нового коронавируса, играет важную роль в процессе репликации и пролиферации вируса и является мишенью при лечении нового коронавируса. Четыре препарата могут ингибировать активность протеазы 3CL, предотвращая репликацию и синтез вирионов нового коронавируса.
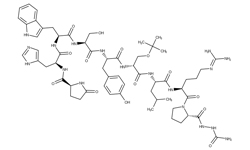
Гозерелин — синтетический аналог рилизинг-гормона лютеинизирующего гормона, используемый для лечения рака молочной железы и рака простаты путем снижения секреции гонадотропинов гипофизом.
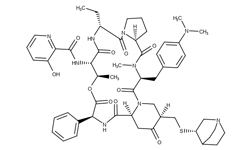
Хинупристин — стрептограминовый антибиотик, используемый для лечения тяжелой ванкомицин-резистентной бактериемии Enterococcus faecium, а также осложненных инфекций кожи.
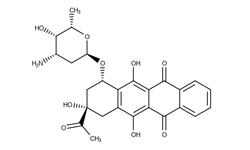
Идарубицин — антрациклиновый антибиотик, цитостатический препарат, аналог даунорубицина. Является противоопухолевым средством, используемым для лечения острого миелолейкоза (ОМЛ) у взрослых.
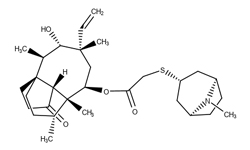
Ретапамулин — антибиотик местного действия, используемый для лечения импетиго, вызванного метициллин-чувствительным Staphylococcus aureus или Streptococcus pyogenes.
Coronavirus main protease inhibitor comprising pyrroloquinoline quinone, coronavirus preventive agent, coronavirus therapeutic agent and coronavirus preventive food
2023.04.21 JP 2023057334 A
Целью настоящего изобретения является создание ингибитора основной протеазы коронавируса, средства профилактики коронавируса, терапевтического средства против коронавируса и пищевого продукта для профилактики коронавируса, который может ингибировать активность основной протеазы коронавируса. Авторы настоящего изобретения провели исследования для решения вышеуказанных проблем и обнаружили, что пирролохинолинхинон, его соли и сольваты ингибируют активность основной протеазы коронавирусов и подавляют коронавирусную инфекцию.
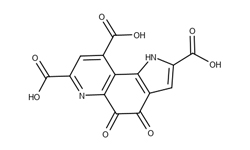
Пирролохинолинхинон, также известный как метоксатин, представляет собой группу протеаз некоторых дегидрогеназ, является окислительно-восстановительным агентом и способен изменять передачу сигнала и поддерживать митохондриальную функцию.
Application of robiniatin in preparation of medicine for treating SARS-CoV-2
2023.07.07 CN 116392473 A
Изобретение относится к применению робиниафлавина как лекарственного средства для лечения SARS-CoV-2. Исследования показывают, что робиниафлавин, соединение относящееся к традиционной китайской медицине, может ингибировать репликацию нового коронавируса и подавлять его активность оказывая ингибирующее действие на протеазу 3CL (Mpro) на уровне белка и живого вируса.
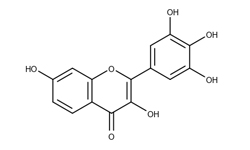
Робинетин (3,3',4',5',7-пентагидроксифлавон) - обладает антиоксидантной и антирадикальной активностью, с высокой эффективностью ингибирует перекисное окисление липидов мембран EYPC и гликозилирование HbA.
Ингибирование РНК-зависимой РНК-полимеразы (RdRp)

Antiviral composition for SARS-CoV-2 and HCoV-OC43 comprising rhein, meclofenamic acid, or a combination thereof
2022.05.27 WO 2022/107999 A1
Настоящее изобретение представляет противовирусную композицию для SARS-CoV-2, включающую реин (Rhein), меклофенаминовую кислоту (Meclofenamic acid) или их комбинацию в качестве активного ингредиента, ингибирующие РНК-зависимую РНК-полимеразу (RdRp).
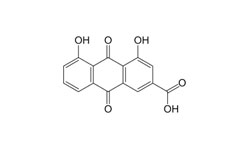
Реин — вещество из группы антрахинонов, обладающее слабительным действием.
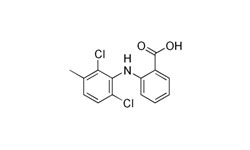
Меклофенаминовая кислота - нестероидный противовоспалительный препарат (НПВП).
Method for inhibiting coronavirus infection and replication
2021.12.16 US 2021/386725 A1
. В настоящем документе раскрыт способ подавления коронавирусной инфекции, включающий введение нуждающемуся в этом субъекту эффективного количества пиоглитазона или его фармацевтически приемлемой соли. Предполагаемый механизм действия - ингибирование РНК-зависимой РНК-полимеразы (RdRp).
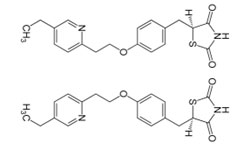
Пиоглитазон — лекарственное средство из класса тиазолидиндионов, используется для снижения уровня глюкозы в крови при сахарном диабете 2 типа.
Pharmaceutical composition for preventing or treating coronavirus disease-19
2022.08.18 US 2022257567 A1
Настоящее изобретение относится к фармацевтической композиции для предотвращения или лечения коронавирусной болезни 2019, найденной с помощью технологии репозиционирования лекарственных средств с использованием технологии виртуального скрининга лекарственных средств. Раскрывается способ профилактики или лечения COVID-19 у нуждающегося в этом субъекта путем введения фармацевтической композиции, включающей либо соединение, специфически связывающееся с Mpro SARS-CoV-2, либо соединение, специфически связывающееся с RdRP SARS-CoV-2, где соединение, специфически связывающееся с Mpro, выбрано из группы, состоящей из алобресиба, CE-326597, блонсансерина и эмодина, и соединение, специфически связывающееся с RdRP, выбрано из группы, состоящей из гиперицина, омипалисиба, LGH-447, NS-3728, типифарниба, валопицитабина, элсамитруцина, NRC-AN-019, денуфосола и изаторибина. В настоящем изобретении соединение, специфически связывающееся с Mpro, предпочтительно представляет собой блонансерин (Blonanserin) или эмодин (Emodin); соединение, специфически связывающееся с RdRP, предпочтительно выбирают из группы омипалисиба (Omipalisib) или типифарниба (Tipifarnib). В результате, как показано в таблице, было подтверждено, что значение IC50 омипалисиба было в 20 раз ниже, чем у ремдезивира, а типифарниб и блонансерин показали значения IC50, аналогичные значениям IC50 ремдезивира. Гиперицин, LGH-447, NS-3728 и эмодин показали более высокие значения IC50, чем ремдезивир, но продемонстрировали значительную противовирусную активность, и, таким образом, эти семь соединений были определены как препараты-кандидаты для лечения COVID-19.
| Target | Drug | IC50 (мкМ) | Target | Drugs | IC50 (мкМ) |
|---|---|---|---|---|---|
| RdRP | Omipalisib | 0.49 мкМ | Mpro | Blonanserin | 11.97 мкМ |
| RdRP | Tipifarnib | 11.01 мкМ | Mpro | Emodin | 31.45 мкМ |
| RdRP | Hypericin | 19.34 мкМ | RdRP(Control) | Remdesivir | 10.09 мкМ |
| RdRP | LGH-447 | 23.91 мкМ | (Control) | Chloroquine | 8.89 мкМ |
| RdRP | NS-3728 | 28.37 мкМ | (Control) | Lopinavir | 11.00 мкМ |
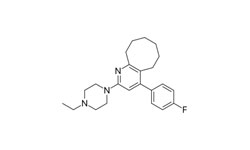
Блонансерин, продаваемый под торговой маркой Lonasen, представляет собой относительно новый атипичный антипсихотик для лечения шизофрении.
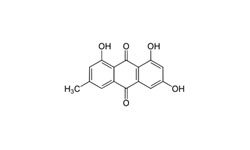
Эмодин - антрахинон, содержащийся в нескольких растениях, проявляет слабительное, антибактериальное и противовоспалительное действие.
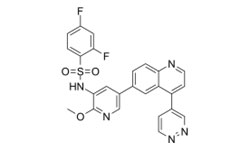
Омипалисиб - это низкомолекулярный ингибитор фосфатидилинозитол-3-киназы (PI3K) с потенциальной антинеопластической активностью.
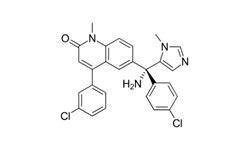
Типифарниб — ингибитор фарнезилтрансферазы с потенциальной антинеопластической активностью.
Application of arenobufagin and derivatives thereof
2022.08.16 CN 114903907 A
Изобретение относится к производному аренобуфагина, представителю активной группы буфотенинов получаемых из экстракта кожи жабы. Производное аренобуфагина получено путем оптимизации его структуры, имеет низкую энергию связывания с белком гидролазы 3CL и ферментом RdRp SARS-CoV-2. Оказывает хорошее ингибирующее действие на вирус SARS-CoV-2.
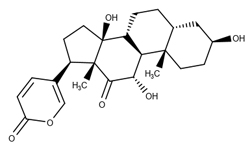
Аренобуфагин — токсин выделяемый жабой Bufo arenarum, используется в китайский народной медицине как противораковое средство.
Compositions and methods utilizing protein inhibitors for synergistic inhibition and treatment of sars-cov-2
2022.04.14 WO 2022076386 A1
Ингибиторы PLpro, в том числе перепрофилированные препараты против гепатита С, такие как гразопревир, ванипревир и паритапревир, увеличивают способность ремдесивира подавлять противовирусную активность репликации коронавируса в 10 раз. Эти композиции могут обеспечить более эффективное лечение пациентов с меньшей токсичностью и побочными эффектами по сравнению с текущими стандартами лечения, а также обеспечить амбулаторное лечение COVID-19 пероральными ингибиторами полимеразы, такими как молнупиравир.
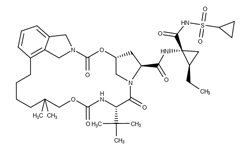
Ванипревир представляет собой макроциклический ингибитор протеазы NS3/4a вируса гепатита С, активен в отношении ферментов протеазы NS3/4a генотипа 1 и генотипа 2.
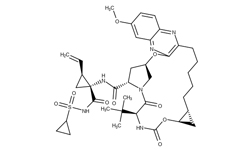
Гразопревир — азамакроциклическое соединение, которое представляет собой ингибитор протеазы гепатита С, для лечения хронической инфекции ВГС генотипов 1 или 4 у взрослых.
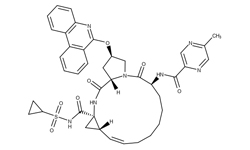
Паритапревир — противовирусное средство прямого действия, используемое в сочетании с другими противовирусными средствами для лечения инфекций, вызванных вирусом гепатита С.
Application of chlorpromazine in preparation of coronavirus inhibitor
2023.08.08 CN 116549456 A
Изобретение раскрывает применение хлорпромазина как ингибитора коронавируса. Изобретение описывает применение хлорпромазина или его фармацевтически активной соли. Эксперименты доказывают, что хлорпромазин обладает хорошей активностью против SARS-CoV-2 и/или против HCoV-OC43 и имеет перспективную основу для лечения инфекции SARS-CoV-2 и/или инфекции HCoV-OC43.
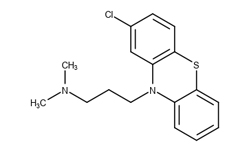
Хлорпромазин — фенотиазиновый антипсихотик, используемый для лечения тошноты, рвоты, предоперационной тревоги, шизофрении, биполярного расстройства и серьезных поведенческих проблем у детей.
Ингибирование папаин-подобной протеазы PLpro коронавируса SARS-CoV-2

Application of PX-12 in preparation of coronavirus papaya-like protease PLPro inhibitor drug
2022.06.14 CN114617877A
Изобретение относится к области медицинской химии, в частности, к применению PX-12 в приготовлении препаратов-ингибиторов папаиноподобной протеазы коронавируса PLPro. PX-12, раскрытый в изобретении, обладает относительно сильным ингибирующим действием на ферментативную активность целевой папаиноподобной протеазы нового коронавируса, и может быть использован для создания препарата против SARS-CoV-2. IC50 = 0.7594 мкМ.
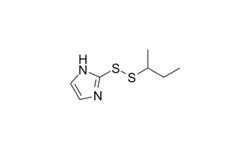
PX-12 (1-methylpropyl-2-imidazolyl-disulfide) является необратимым ингибитором тиоредоксина-1 (Trx-1); индуцирует апоптоз; ингибирует миграцию и инвазию клеток колоректального рака.
Application of Succimer in preparation of anti-coronavirus infection medicine and medicine
2022.03.29 CN114246854A
Изобретение относится к области медицинской химии и, в частности, касается применения сукцимера (Succimer) и его фармацевтически приемлемой соли в приготовлении лекарственных средств против коронавирусной инфекции. Сукцимер обладает сильным ингибирующим действием на ферментативную активность папаиноподобной протеазы Plpro, мишени коронавируса, особенно нового коронавируса, и может быть использован для приготовления лекарства против SARS-CoV-2. IC50 = 369,3 нМ.
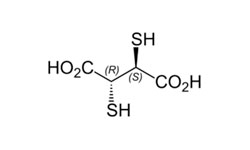
Сукцимер, продаваемый, среди прочего, под торговой маркой Chemet, представляет собой лекарство, используемое для лечения отравлений свинцом, ртутью и мышьяком.
Ингибирование сериновой протеазы TMPRSS2

Application of aerosol allicin in prevention and treatment of new coronavirus infection and other respiratory tract infectious diseases
2020.11.13 CN111920786A
Настоящее изобретение относится к области медицины, в частности к применению аэрозольного аллицина для профилактики и лечения SARS-CoV-2 и других инфекционных заболеваний дыхательных путей. Пары аллицина могут эффективно ингибировать TMPRSS2 и блокировать проникновение и заражение клеток новым коронавирусом, а также устранить инфекционные факторы в альвеолярном воздухе для достижения эффективной профилактики и лечения.
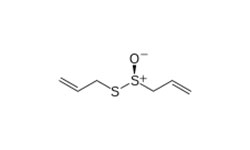
Аллицин — органическое соединение, сульфоксид, которое образуется при механическом разрушении клеток чеснока, обладающее бактерицидным и фунгицидным действием.
Лиганды рецептора сигма-1 (σ1R)

Sigma receptor ligands for treating SARS-CoV-2 infection
2022.08.11 WO 2022/169961 A1
В настоящем документе раскрываются методы лечения или предотвращения инфекции SARS-CoV-2 у субъекта, включающие введение субъекту соединения или его соли, обладающей сродством к связыванию с сигма-рецептором. Представлены соединения AZ66, CM304, CM398 и SA4503 или их соли, показавшие значительную ингибирующую активность. Из всех лигандов, протестированных в данной работе, наибольшую активность проявил AZ66 (EC50 = 15.93 мкМ).
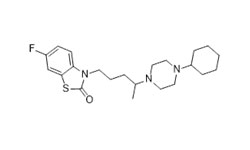
AZ66 - смешанный антагонист сигма-1/сигма-2 рецепторов.
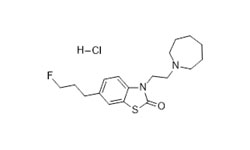
CM304 является высокоселективным антагонистом сигма-1 рецепторов.
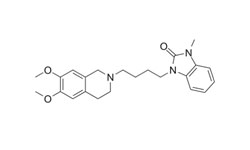
CM398 является высокоселективным, активным лигандом сигма-2 рецепторов.
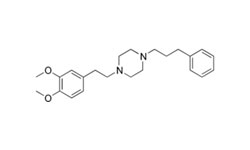
SA4503 является селективным агонистом сигма1-рецепторов.
Treatment of viral infection, disease or disorder using a selective S1R agonist
2021.11.11 CA 3176917 A1
Данное изобретение относится к способу лечения вирусного заболевания COVID-19 у нуждающегося в этом субъекта, включающий введение субъекту селективного агониста сигма-1 рецепторов придопидина (Pridopidine) или его фармацевтически приемлемой соли. Придопидин представляет собой низкомолекулярный исследуемый препарат для перорального применения и находится на поздней стадии клинической разработки для лечения болезни Хантингтона и бокового амиотрофического склероза (БАС).
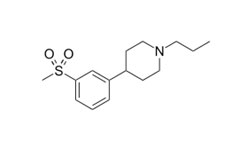
Придопидин является селективным и мощным агонистом рецепторов сигма-1.
Не вирусные мишени или информация о мишенях отсутствует

Uses of propranolol for managing viral infections
2023.03.09 WO 2023034282 A1
Настоящее изобретение относится к способам лечения или профилактики вирусной инфекции, такой как SARS-CoV-2, включающим введение эффективного количества пропранолола, пролекарств или его солей пациенту, нуждающемуся в этом.
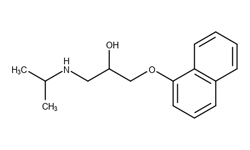
Пропранолол — неселективный β-адренергический антагонист, используемый для лечения гипертензии, стенокардии, фибрилляции предсердий, инфаркта миокарда, мигрени, эссенциального тремора, гипертрофического субаортального стеноза и феохромоцитомы.
Diosmetin for treatment of human coronavirus infection
2023.04.12 EP 4162935 A1
Изобретение относится к использованию диосметина для лечения коронавирусной инфекции, в частности SARS-CoV-2 и его вариантов (например, альфа, бета, гамма, дельта, омикрон и других).
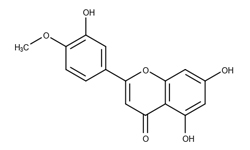
Диосметин представляет собой O-метилированный флавон и агликоновую часть флавоноидного гликозида диосмина, который в природе встречается в цитрусовых. Сообщается, что с фармакологической точки зрения диосметин проявляет противораковую, противомикробную, антиоксидантную, эстрогенную и противовоспалительную активность. Он также действует как слабый агонист рецептора TrkB 1.
Application of linagliptin in preparation of coronavirus drugs
2023.09.12 CN 116726023 A
Раскрыто применение линаглиптина при приготовлении лекарственного средства для профилактики коронавируса или ингибирования инвазии коронавируса (HCoVn o229E, HCoV-NL63, HCoV-OC43, HCoV-HKU1, MERS-CoV, SARS-CoV, SARS-CoV-2, альфа-вариант SARS-CoV-2 и т.д.). Лекарство можно приготовить в виде раствора для инъекций, таблетки и т. д. Линаглиптин может безопасно и эффективно противостоять инвазии коронавируса, не влияя на жизнеспособность клеток-хозяев.
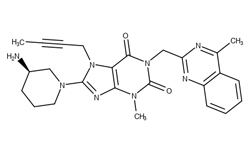
Линаглиптин — ингибитор дипептидилпептидазы-4, используемый для лечения гипергликемии у пациентов с сахарным диабетом 2 типа.
Rimegepant for treatment of human coronavirus infection
2023.03.22 EP 4151214 A1
Изобретение относится к применению римегепанта или его фармацевтически приемлемой соли для лечения инфекции, вызываемой коронавирусом человека, а именно SARS-CoV-2 и его вариантов (например, альфа, бета, гамма, дельта, омикрон и другим).
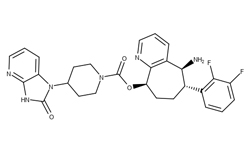
Римегепант — пероральный антагонист рецепторов CGRP, используемый для лечения мигрени с аурой или без нее у взрослых.
Application of antibacterial peptide Indolicidin in preparation of anti-coronavirus drugs
2023.11.17 CN 117065000 A
Изобретение относится к применению противомикробного пептида индолицидина, который эффективно ингибирует действие SARS-COV-2 в клеточных линиях со сверхэкспрессией 293T ACE2 и H1299ACE2; препарат по настоящему изобретению оказывает значительное влияние на коронавирус 2019-nCoV, HCoV-229E, HCoV-OC43, SARS-CoV и/или MERS- CoV.
Индолицидин, член семейства белков кателицидинов, представляет собой катионный антимикробный пептид-амид из 13 остатков, выделенный из цитоплазматических гранул бычьих нейтрофилов. Индолицидин оказывает микробицидное действие in vitro против грамположительных и грамотрицательных бактерий, грибов, простейших и вируса иммунодефицита человека (ВИЧ-1).
Application of isoliquiritigenin in preparation of medicine for preventing and treating coronavirus infection
2023.04.14 CN 115957201 A
Инновация настоящего изобретения заключается в том, что изоликвиритигенин обладает ингибирующей способностью репликации коронавируса (SARS-CoV-2), а так же HCoV-OC43 и HCoV-229E. Настоящее изобретение заявляется как основа для разработки противокоронавирусных препаратов и обеспечивает новую схему медикаментозного лечения в клинических условиях и профилактических целях.
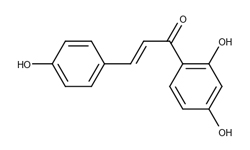
Изоликвиритигенин - представляет собой халкон, который обладает антиоксидантным, противовоспалительным, противовирусным, противодиабетическим, спазмолитическим и противоопухолевым действием.
Combination of cetylpyridinium and benzydamine with virucidal effect on SARS-COV-2
2023.03.30 WO 2023046680 A1
Изобретение относится к фармацевтической лекарственной форме, содержащей физиологически подготовленную соль цетилпиридиния и бензидамин, предназначеной для лечения и/или профилактики коронавирусной инфекции.
Цетилпиридиний — это соединение, используемое для уменьшения зубного налета и гингивита, а также для отбеливания зубов. Бензидамин — НПВС местного действия, показанное для симптоматического облегчения острой боли в горле и для симптоматического облегчения мукозита ротоглотки, вызванного лучевой терапией.
Application of ametinib in preparation of anti-coronavirus medicine
2023.11.17 CN 117064893 A
Изобретение относится к применению аметиниба при приготовлении противокоронавирусного препарата. Эксперименты in vivo и in vitro доказывают, что аметиниб Альмонертиниб может значительно снизить эффективность заражения SARS-COV-2 и препятствовать проникновению вируса в клетки, оказывая ингибирующее действие по крайней мере на один из коронавирусов: 2019-nCoV, HCoV-229E, HCoV-OC43, SARS-CoV и MERS-CoV. Соединение может быть использованоо для приготовления лекарственных средств для лечения коронавируса и его осложнений, в том числе простой инфекционной лихорадки, кашля и боли в горле, пневмонии, острой инфекции дыхательных путей, тяжелой острой респираторной инфекции, гипоксической дыхательной недостаточности, острого респираторного дистресс-синдрома, сепсиса и септического шока.
Альмонертиниб представляет собой ингибитор тирозинкиназы EGFR третьего поколения, нацеленный на сенсибилизирующие EGFR и резистентные к T790M мутации. Его исследуют в отношении распространенного или метастатического немелкоклеточного рака легких с мутацией EGFR.
Entospletinib for use in the treatment of COVID-19 patients
2023.11.17 WO 2023144353 A1
Изобретение относится к энтосплетинибу (GS-9973) или его фармацевтически активной соли, сложному эфиру или производному для применения при лечении коронавирусной инфекции.
Энтосплетиниб - используется в исследованиях по лечению онкологии, фолликулярной лимфомы, B-клеточных злокачественных новообразований, лимфомы мантийных клеток и неходжкинской лимфомы.
Methods for treating coronavirus infection
2023.01.19 WO 2023287620 A1
Способы лечения коронавирусной инфекции у пациента, которые включают введение терапевтически эффективного количества агента, составленного из одного или нескольких веществ: артесуната, дигидроартемизинина, изорамнетина, ликорина, (+)-таксифолина, байкалина, таншинона I и дезэтиламодиахина. Представлены фармацевтические композиции, включающие фармацевтическую дозу двух или более агентов, выбранных из группы, состоящей из: артесуната, дигидроартемизинина, изорамнетина, ликорина, (+)-таксифолина, байкалина, таншинона I, дезэтиламодиахина, артемизинина, нирмателвира и ритонавира, нирмарелвира, ритонавира, байкалеина, рамнетина, (-)-таксифолина и криптотаншинона.
Артесунат — это производное артемезинина, предназначенное для начального лечения тяжелой малярии.
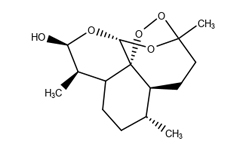
Дигидроартемизинин — производное артемизинина, является противомалярийным средство, используемым для лечения неосложненных инфекций вызываемых малярийным плазмодием (Plasmodium falciparum).
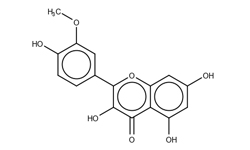
Изорамнетин представляет собой О-метилированный флавонол из класса флавоноидов.
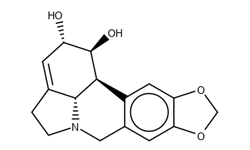
Ликорин обладает антибактериальной, противовирусной и противовоспалительной активностью, в том числе обладает ингибирующим свойством в отношении нескольких линий раковых клеток.
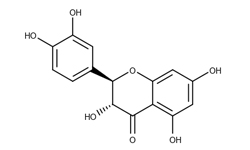
Таксифолин - изомер дигидрокверцетина транс (2R,3R)-дигидрокверцетин, действует как потенциальный химиопрофилактический агент, регулируя гены посредством ARE-зависимого механизма.
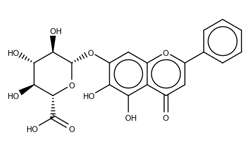
Байкалин вместе с его агликоном байкалеином является положительным аллостерическим модулятором бензодиазепинового сайта и/или небензодиазепинового сайта ГАМКА-рецептора.
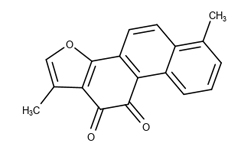
Таншинон I обладает противовоспалительным действием, а также модулирует или предотвращает метастазирование рака молочной железы путем регулирования молекул адгезии.
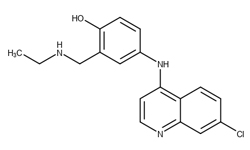
Дезэтиламодиахин - активная форма препарата амодиахина, лекарственного средства, используемого для лечения малярии, включая неосложненную малярию Plasmodium falciparum.
Application of ASGR1 competitive binding agent in preparation of preparation for inhibiting SARS-CoV-2 from infecting host cells
2023.07.28 CN 116492352 A
Изобретение относится к новому медицинскому применению конкурентно-связывающего агента ASGR1 и, в частности, относится к группе химических лекарственных средств для предотвращения заражения клеток хозяина SARS-CoV-2 через белок ASGR1. Конкурентно-связывающим агентом ASGR1 является галактоза и галактозамин. Согласно настоящему изобретению, результаты испытаний показывают, что галактозу можно комбинировать с потенциальным рецептором Covid-19 ASGR1, чтобы предотвратить попадание Covid-19 в клетку-хозяина.
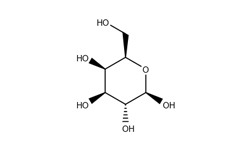
Галактоза - моносахарид из группы гексоз, заявлена в исследованиях по изучению лечения и диагностики гепатита С, рака печени, болезни Вильсона, диабетического макулярного отека, фокального сегментарного гломерулосклероза и др.
Use of Rigosertib to treat RNA virus infections
2021.12.02 WO 2021/243162 A1
В настоящем документе раскрывается метод лечения инфекции SARS-CoV-2 или COVID- 19, включающий введение субъекту, нуждающемуся в этом, эффективного количества ригосертиба (Rigosertib). Модулируя путь RAS/RAF/MEK/ERK, участвующий в пролиферативной сигнализации, ригосертиб может играть важную роль в подавлении репликации COVID-19 в клетках человека, в частности, в легочной ткани, являющейся основным источником серьезного заболевания. Ригосертиб демонстрирует впечатляющее ингибирование репликации SARS-CoV-2 в клетках Vero с IC50 16 нМ.
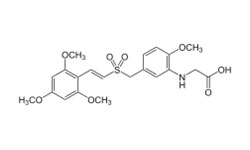
Ригосертиб - мультикиназный ингибитор и селективное противораковое средство, находится в фазе III клинических испытаний для лечения хронического миеломоноцитарного лейкоза.
TGF-Bβ1 inhibitors for preventing and treating SARS-CoV-2
2021.09.30 WO 2021/195088 A1
Раскрывается метод профилактики или лечения инфекции SARS-CoV-2 у нуждающегося в этом субъекта, включающий введение субъекту терапевтически эффективного количества по меньшей мере одного ингибитора трансформирующего фактора роста бета 1 (TGF- beta1), который блокирует взаимодействие TGF- beta1 и SARS-CoV-2 NSP15. Были выбраны ингибиторы Galunisertib (LY2157299), LY580276, LY550410, SB505124, GS-1423, AVID200, Fresolimumab, LY2382770, LY3022859 и XOMA089, и определены соответствующие концентрации ингибиторов для оценки их способности блокировать эффект опосредованной белком SARS-CoV-2 NSP15 активации латентного TGF- beta1. GS-1423, AVID200, Фрезолимумаб, LY2382770, LY3022859, XOMA089 - моноклональные антитела, находятся на различных стадиях испытаний для применения в противораковой терапии.
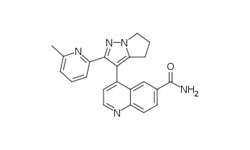
Галунисертиб - экспериментальный противораковый препарат, исследовался для лечения гепатоцеллюлярной карциномы.
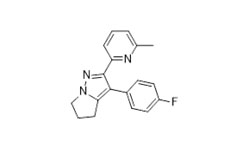
LY580276 - ингибитор TGF- beta1, исследуется для противораковой терапии.
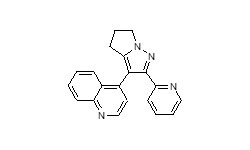
LY550410- ингибитор TGF- beta1 с потенциальной противораковой активностью.
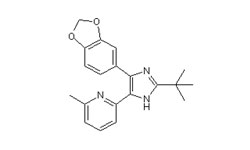
SB505124 - селективный ингибитор TGF- beta1 с потенциальной противораковой активностью.
Application of andrographolide in preparation of product for treating coronavirus infection
2022.03.29 CN114246859A
Изобретение раскрывает применение андрографолида (Andrographolide) или его фармацевтически приемлемой соли для ингибирования коронавируса SARS-CoV-2. EC50, CC50 и SI = 5.285 мкМ, >50мкМ, >9.46, соответственно.
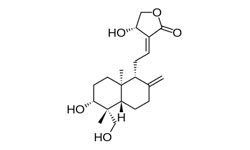
Андрографолид — натуральный лабдановый дитерпеноид, выделенный из стебля и листьев андрографиса метельчатого, применяется в народной медицине в Юго-восточной Азии.
Application of andrographolide in preparation of product for treating coronavirus infection
2022.03.29 CN114246874A
Объектом настоящего изобретения является применение рускогенина (Ruscogenin) или его фармацевтически приемлемой соли для подавления коронавируса SARS-CoV-2 и предотвращения коронавирусной инфекции. Результаты исследования показывают, что рускогенин обладает хорошей противовирусной активностью, низкой токсичностью и побочными эффектами, и имеет потенциальное клиническое применение. EC50, CC50 и SI составили 11,70 мкМ, >50 мкМ, >4,27, соответственно.
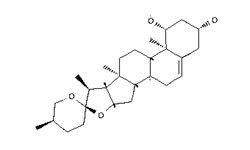
Рускогенин - это природное соединение, применяемое в традиционной китайской медицине.
Application of isoferulic acid in preparation of product for preventing and treating coronavirus infection
2022.03.29 CN114246853A
Изобретение раскрывает применение изоферуловой кислоты (isoferulic acid) или ее фармацевтически приемлемой соли для ингибирования коронавируса SARS-CoV-2. Результаты исследования показывают, что изоферуловая кислота обладает хорошей противовирусной активностью, низкой токсичностью и побочными эффектами, и имеет потенциальное клиническое применение. EC50, CC50 и SI составили 13,63 мкМ, >50 мкМ, 3,67, соответственно.
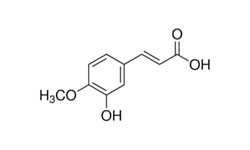
Изоферуловая кислота - природное соединение, применяемое в традиционной китайской медицине.
Methods and pharmaceutical compositions of Thromboxane A2 receptor antagonist for the treatment of COVID-19
2021.10.07 CA 3176619 A1
Настоящее изобретение относится к применению антагонистов рецептора тромбоксана A2, в частности, ифетробана (Ifetroban) и их фармацевтических композиций в эффективном количестве для лечения инфекции SARS-CoV-2 (например, COVID-19) у млекопитающих (например, людей) с целью лечения этого заболевания. Ифетробан был изучен на животных моделях для лечения метастазов рака, ишемии миокарда, гипертонии, инсульта, тромбоза, кардиомиопатии, и для воздействия на тромбоциты.
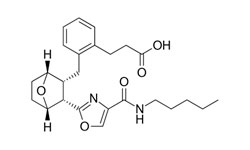
Ифетробан является мощным и селективным антагонистом тромбоксановых рецепторов.
A Chlorophyllin containing pharmaceutical composition for prevention of pathogenesis of coronavirus disease
2022.09.21 EP4059493 A1
Настоящее изобретение относится к фармацевтической композиции для предотвращения патогенеза коронавирусной инфекции и заболевания у человека. Указанная фармацевтическая композиция включает хлорофиллин (Chlorophyllin) или его соли и направлено на лечение состояний, включающих коронавирусную инфекцию, подавление иммунитета, лейкопению и лимфопению. Исследования in vitro показывают, что хлорофиллин ингибирует размножение вируса SARS-CoV-2. Было установлено, что концентрация хлорофиллина, необходимая для ингибирования роста вируса SARS-CoV-2 на 50% (EC50), составляет менее 1 мкМ.
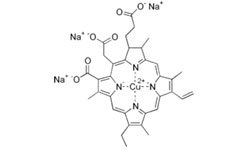
Хлорофиллин - средство растительного происхождения.
Lidocaine or Articaine for treating COVID-19, autoimmune disease or cytokine storm response
2022.12.08 WO 2022254363 A1
Настоящее изобретение относится к высокодозному/малообъемному составу лидокаина, или его соли, или артикаина, или его соли, для использования в лечении COVID-19 или аутоиммунного заболевания или состояния, при котором иммунный ответ, вызванный заболеванием или инфекцией, вызывает цитокиновый шторм. Введение лидокаина, направленное на лимфатическую систему субъекта, оказывается наиболее эффективным при лечении COVID-19. Оптимальным является применение единичной дозы лидокаина высокой концентрации в небольшом объеме (менее 0,5 мл), превышающей 10%.
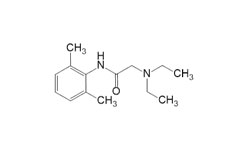
Лидокаин — лекарственное средство, местный анестетик и сердечный депрессант
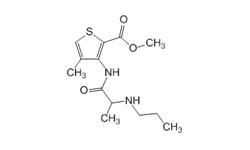
Артикаин является местноанестезирующим средством амидного типа.
Lauryl gallate for use as antiviral agent
2022.12.21 EP4104829 A1
Изобретение относится к новому применению лаурил галлата (Lauryl gallate), его таутомеров и/или сольватов в качестве противовирусного агента для лечения и/или профилактики коронавирусных инфекций и, в частности, коронавирусных инфекций человека. В случае SARS-CoV-2 диапазон ингибирования был получен как в клеточных линиях Vero-E6 (IC50 =1,281 мкМ), так и в Caco-2 (IC50 =2,977 мкМ). Лаурилгаллат используется в качестве пищевой добавки под номером E E312 как антиоксидант и консервант.
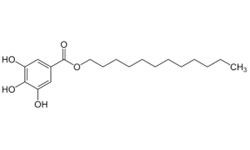
Лаурилгаллат представляет собой сложный эфир додеканола и галловой кислоты.
Methylene blue and Riboflavin for prophylactic and therapeutic anti-viral therapy
2021.12.23 WO 2021254928 A11
Настоящее изобретение описывает использование метиленового синего (Methylene Blue) и рибофлавина (Riboflavin), двух одобренных FDA препаратов с отличным профилем безопасности. С помощью анализа нейтрализации вирусов гриппа H1N1 A и SARS-CoV-2 продемонстрирована значительная вирулицидная активность обоих препаратов в фармакологической дозе. Описано профилактическое и терапевтическое противовирусное использование препаратов in vivo. Метиленовый синий относится к списку жизненно важных препаратов ВОЗ для лечения метгемоглобинемии (антидот при отравлении цианидами, угарным газом и сероводородом); имеются сообщения о высокой эффективности этого соединения при лечении болезни Альцгеймера. Рибофлавин используют при кожных заболеваниях, вяло заживающих ранах, заболеваниях глаз, нарушении функции желудочно-кишечного тракта, диабете, анемиях, циррозе печени.
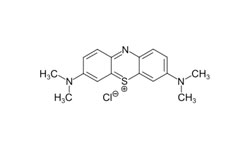
Метиленовый синий - тиазиновый краситель использующийся в медицине в качестве антисептика.
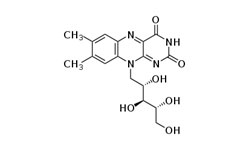
Рибофлавин применяют для профилактики и лечения недостаточности витамина B2 и сопутствующих этому заболеваниях.
Применение дигидрохлорида N,N'-бис-(2,3-бутадиенил)-1,4-диаминобутана (MDL72.527) для подавления репродукции вируса SARS-CoV-2
2021.12.10 RU0002761565
Изобретение относится к области вирусологии, фармакологии и биоорганической химии, конкретно к применению вещества - дигидрохлорида N,N'-бис-(2,3-бутадиенил)-1,4-диаминобутана (MDL72.527) - для подавления репликации коронавируса SARS-CoV-2. Подавление осуществляется за счет ингибирования катаболизма биогенных полиаминов. MDL72.527 подавляет репродукцию SARS-CoV-2 в микромолярных концентрациях, снижая уровни его РНК в культуральной среде. Изобретение может найти применение при лечении новой коронавирусной инфекции, вызываемой SARS-CoV-2.
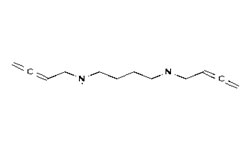
MDL72.527 - ингибитор полиаминоксидазы, который проявляет противораковую и нейропротекторную активность in vivo.
Use Of Tafenoquine, Boceprevir Or Narlaprevir For Treating Infection Of SARS-COV-2 And Medical Composition Thereof
2022.02.03 US 2022031709 A1
Данное изобретение в целом относится к ингибированию микросомальной простагландин E2 (PGE2 ) синтазы-1 (mPGES-1). В частности, некоторые варианты реализации раскрытого объекта относятся к использованию цефтриаксона (Ceftriaxone), азтреонама (Aztreonam), цефотетана (Cefotetan) и их фармацевтически приемлемых солей в качестве ингибиторов mPGES-1. Раскрывается также способ лечения коронавируса SARS-CoV-2, включая защиту от коронавирусной инфекции или снижение риска ее возникновения и/или лечение коронавирусной инфекции, который включает введение субъекту эффективного количества селективного ингибитора mPGES-1, выбранного из группы, состоящей из цефтриаксона, азтреонама, цефотетана, и фармацевтически приемлемых их солей.
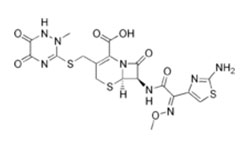
Цефтриаксон — антибиотик цефалоспоринового ряда широкого спектра действия.
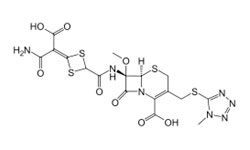
Цефотетан известен как антибиотик цефамицинового ряда.
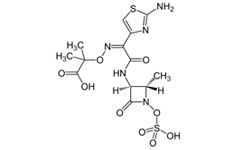
Азтреонам - бета-лактамный антибиотик против аэробных грамотрицательных бактерий.
Drug ranking method and system, comparison method for drug ranking method, correction method for drug ranking method
2023.01.18 EP4120277
В данном документе представлен способ отбора лекарственных средств, которые могут быть повторно использованы для лечения заболеваний или симптомов (например, вызванных инфекцией SARS-CoV-2), отличных от их известных показаний. Было показано, что тегасерод (Tegaserod) и фенотерол (Fenoterol) являются перспективными кандидатами для лечения инфекции SARS-CoV-2. EC50 фенотерола для инфицированных SARS-CoV-2 клеток Vero E6 составляла 30 мкМ, а EC50 тегасерода для инфицированных SARS-CoV-2 клеток Vero E6 была немного ниже 10 мкМ.
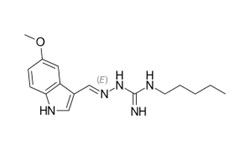
Тегасерод — агонист 5-HT4, применяется для лечения синдрома раздраженного кишечника и запоров.
Фенотерол - применяют для лечения и профилактики бронхиальной астмы, астматического и хронического бронхитов.
Methods involving neutrophil elastase inhibitor Alvelestat for treating coronavirus infection
2021.10.21 WO 2021209740 A1
Настоящее изобретение относится к новым методам лечения коронавирусной инфекции (например, SARS-CoV- 2/COVID-19), ее симптомов и осложнений, а также состояний, связанных с такой инфекцией, включающим введение ингибитора эластазы нейтрофилов, в частности, алвелестата (Alvelestat) или фармацевтически приемлемой соли и/или сольвата, субъекту, нуждающемуся в этом.
Алвелестат — селективный и обратимый ингибитор эластазы нейтрофилов человека (NE), проявляет потенциальную противоопухолевую активность.
Применение даларгина для производства средств лечения коронавирусной инфекции COVID-19
2020.03.08 RU 2728939 C1
Изобретение относится к области фармакологии и медицины и предназначено для лечения коронавирусной инфекции COVID - 19 . Для лечения COVID - 19 применяют Даларгин (гексапептид формулы H-Tyr-D-Ala-Gly-Phe-Leu-Arg-OH ) или его фармацевтически приемлемую соль. Использование изобретения обеспечивает эффективное лечение симптомов COVID - 19 . Терапевтически эффективное количество гексапептида составляет от 0,01 до 1 мг/кг веса тела субъекта.
Даларгин - противоязвенный препарат; синтетический гексапептид, аналог лейцинэнкефалина.
Способ лечения Ковид 19
2022.08.08 RU 2777645 C1
Изобретение относится к области медицины и может быть использовано для лечения Covid 19 . Предлагаемый способ лечения Covid 19 заключается в том, что больному с легким, среднетяжелым и тяжелым течением заболевания проводят внутримышечные инъекции раствора Унитиола (Unithiol) или Димеркапрола (Dimercaprol) 50 мг/мл по разработанной схеме. Предложенное изобретение направлено на излечение больного.
Унитиол - антидот, донатор сульфгидрильных групп, взаимодействуя с тиоловыми ядами (соединения мышьяка, соли тяжелы металлов) и образуя с ними нетоксичные, водорастворимые соединения.
Димеркапрол, также «Британский антилюизит» (BAL), — дезинтоксикационное лекарственное средство, сходное с унитиолом; подобно унитиолу оказывает антидотное действие.
Мефлохин и его комбинации для лечения и профилактики коронавирусной инфекции
2021.24.12 RU 2763024 C1
Изобретение относится к области медицины и фармацевтики, а именно к применению мефлохина (Mefloquine) в качестве лекарственного агента против инфекции, вызванной вирусом SARS-CoV-2, в количестве 500 мг мефлохина в сутки, в течение четырех дней лечения. Предпочтительно, введение осуществляют два раза в сутки перорально или гастроэнтерально. Изучение противовирусной активности мефлохина проводили в системах in vitro на культурах клеток почки зеленой мартышки линии Vero E6. Мефлохин полностью предотвращал цитопатическое действие вируса SARS-CoV-2 в культуре клеток в концентрации 4,7 мкМ, что составляет 2,0 мкг/мл.
Мефлохин, также Лариам — лекарство, используемое для профилактики или лечения малярии.
Application of taurolidine in preparation of anti-novel coronavirus SARS-CoV-2 medicine
2020.10.16 CN111773227A
Изобретение относится к применению тауролидина (Taurolidine) в приготовлении препарата против нового коронавируса SARS-CoV-2 и относится к технической области лекарственных средств. В изобретении впервые обнаружено новое применение тауролидина, а именно, применение тауролидина для ингибирования нового коронавируса SARS-CoV-2. Клинической практикой выявлена безопасность тауролидина для организма человека, обнаружено очевидное лекарственное действие тауролидина на новый коронавирус SARS-CoV-2, создана мощная теоретическая база и мощная практическая база для противодействия новому коронавирусу COVID-19, обеспечена ценность разработки и популяризаторское значение. Изобретение обеспечивает новый способ лечения COVID-19.
Тауролидин - синтетический антибиотик широкого спектра действия с антибактериальной, антикоагулянтной и потенциальной антиангиогенной активностью.
Application of endoximol hydrochloride in preparation of medicine for treating diseases caused by novel coronavirus
2022.05.13 CN114469912A
Изобретение раскрывает применение гидрохлорида эндоксифена (Endoksifen) в приготовлении препаратов для лечения заболеваний, вызванных SARS-CoV-2. Это низкомолекулярное соединение имеет преимущества низкой токсичности и высокой эффективности и может ингибировать репликацию нового коронавируса SARS-CoV-2 дозозависимым образом. Его CC50 составляет 124,7 мкМ, IC50 составляет 0,91 мкМ, индекс селективности (SI) составляет около 137.
Эндоксифен - лиганд рецептора эстрогена α (ERα); мощный антиэстроген; метаболит тамоксифена. Он также оценивается как антипсихотик для лечения мании и других психотических расстройств.
Application of clofazimine to preparation of medicines for resisting novel coronavirus infectious diseases
2021.02.09 CN112336724A
Изобретение раскрывает применение клофазимина (Clofazimine) для приготовления лекарств для противодействия новым коронавирусным инфекционным заболеваниям, в частности, SARS-CoV-2. Результаты определения цитотоксичности клофазимина и противовирусной активности на клетках VeroE6 в отношении новых коронавирусов демонстрируют высокий эффект противодействия вирусам на клеточном уровне. CC50 клофазимина на клетках Vero E6 составляет >100 мкМ, IC50 = 0.07694 мкМ.
Клофазимин, продаваемый под торговой маркой Lamprene, представляет собой лекарство, используемое вместе с рифампицином и дапсоном для лечения проказы.
Applications of salvianolic acid B or pharmaceutically acceptable salt thereof in preparation of anti-SARS-CoV-2 drugs
2021.03.19 CN112516131A
Изобретение раскрывает применение сальвианоловой кислоты B (salvianolic acid B) или фармацевтически приемлемой ее соли в приготовлении препаратов против SARS-CoV-2. Продемонстрирован значительный эффект противодействия вирусам на клеточном уровне: IC50 = 0.42 мкМ, EC50=55,47 мкМ.
Сальвианоловая кислота B - натуральный продукт, один из основных активных компонентов Salvia miltiorrhiza (красный шалфей или китайский шалфей), обладающий антиоксидантным действием.
Application of protoporphyrin in preparation of medicine for resisting novel coronavirus SARS-CoV-2
2021.10.26 CN113546077A
Изобретение относится к области медицины и касается нового медицинского применения протопорфирина, в частности, применения протопорфирина IX (Protoporphyrin IX) в приготовлении лекарства для противодействия новому коронавирусу SARS-CoV-2. Эксперименты доказывают, что инфекция нового коронавируса может быть эффективно подавлена путем вмешательства протопорфирина в культуру клеток Vero-E6 (клетки почек африканской зеленой мартышки) in vitro. IC50 = 1.25 мкМ, EC50=0,227 мкМ, CC50=219,1 мкМ.
Протопорфирин IX — органическое вещество класса порфиринов; играет важную роль в живых организмах как предшественник других важнейших соединений, таких как гемоглобин и хлорофилл.
Treatment or prevention of SARS-CoV-2 infection using (S)-crizotinib
2023.02.09 WO 2023015197
Изобретение в целом относится к лечению или профилактике инфекции SARS-CoV-2 и, в частности, к использованию (S)-кризотиниба (S)-crizotinib) или его фармацевтически приемлемой соли в таком лечении или профилактике путем введения пациенту эффективной дозы.
Кризотиниб - продаваемый, в частности, под торговой маркой Xalkori, представляет собой противоопухолевый препарат, используемый для лечения немелкоклеточной карциномы легких.
Application of small molecule compound piperifoside in preparation of SARS-CoV-2 resisting medicine
2022.05.20 CN114515291A
Изобретение раскрывает применение низкомолекулярного соединения Перифозин (Perifosine) в приготовлении лекарства для противодействия коронавирусу SARS-CoV-2. Согласно изобретению, для выявления анти-SARS-CoV-2 активности пиперифена использовали восприимчивую клеточную линию SARS-CoV-2, включая клетки почек африканской зеленой мартышки Vero E6 (EC50 = 0,7227 мкМ) и клетки аденокарциномы легких человека Clu-3 (EC50 = 0,7579 мкМ). Результаты экспериментов показывают, что перифозин может эффективно подавлять инфекцию SARS-CoV-2 на восприимчивых клетках, обладает относительно низкой цитотоксичностью, может быть использован в качестве лекарства для эффективного противостояния инфекции SARS-CoV-2 и имеет перспективу применения.
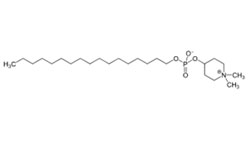
Перифозин — селективный биодоступный ингибитор Akt и PI3K, проявляет потенциальную противоопухолевую активность.
Anti-SARS-CoV-2 agent
2021.12.13 JP2021187761
Изобретение раскрывает применение низкомолекулярного соединения Сенекривирок (Cenicriviroc) или его фармацевтически приемлемой соли в приготовлении лекарства для противодействия коронавирусу SARS-CoV-2. Согласно настоящему изобретению, Сенекривирок обладает значительной активностью и может быть использован в качестве препарата для SARS-CoV-2. (EC50 = 19,0±0,2 мкМ, CC50>40 мкМ).
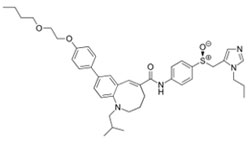
Сенекривирок (Cenicriviroc, CVC, TAK-652, TBR-652)— новый антиретровирусный препарат, экспериментальный кандидат для лечения ВИЧ-инфекции, является ингибитором CCR5 и CCR2 рецепторов.
Composition for prevention and early treatment of viral infection
2022.03.25 CN114224896A
Настоящее изобретение относится к фармацевтической композиции для профилактики и раннего лечения вирусной инфекции, в частности, к применению и способу лечения ингибиторами ионных каналов кальция, а именно, дилтиаземом (Diltiazem). Показано, что дилтиазем ингибирует TMPRSS2-зависимое слияние мембран во время инфекции SARS-CoV-2; он может подавлять активацию кальциевого канала L-типа Cav1.2α1c. Исследование показывает, что Cav1.2α1c является еще одной мишенью для разработки противовирусных препаратов, взаимодействуя с SARS-CoV-2 S белком и ACE2. CC50 дилтиазема на клетках Vero E6 составляет 279,2 мкМ, IC50 = 11,99 мкМ.
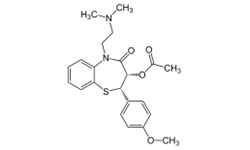
Дилтиазем — блокатор кальциевых каналов, обладает антиангинальным, антиаритмическим и гипотензивным эффектами.
Formulations and methods of treating COVID-19 and preventing infection with SARS-CoV-2
2022.02.17 WO 2022035558 A1
Предлагается метод лечения COVID-19, включающий: ежедневное введение нуждающемуся в этом человеку терапевтически эффективной дозы мифепристона (Mifepristone) или его фармацевтически приемлемой соли и/или аналога и терапевтически эффективной дозы амлодипина (Amlodipine) или его фармацевтически приемлемой соли.
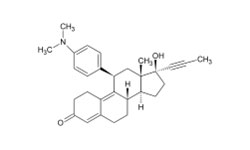
Мифепристон — синтетическое стероидное антипрогестагенное лекарственное средство.
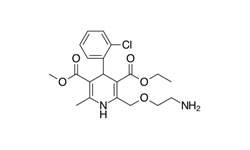
Амлодипин — блокатор медленных кальциевых каналов 2-го поколения.
Application of osimertinib to inhibitor for resisting novel coronavirus infection
2021.12.31 CN113855677A
Изобретение относится к области биомедицины, в частности, к применению осимертиниба (Osimertinib) в качестве ингибитора инфекции SARS-CoV-2. В ходе эксперимента по целевому скринингу лекарственных средств было установлено, что противоопухолевый препарат осимертиниб, может связываться с аминокислотным участком домена RBD белка-шипа нового коронавируса (SARS-CoV-2), а антивирусный эффект достигается путем конкурентного ингибирования комбинации структурного домена и рецептора ACE2 клетки-хозяина. Было показано что препарат может подавлять репликацию диких штаммов вируса в восприимчивых клетках с IC50 около 1,19 мкМ, и обладает определенной цитотоксичностью выше 5 мкМ.
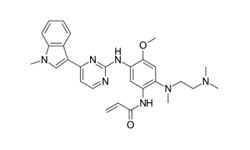
Осимертиниб - противоопухолевое средство, ингибитор тирозинкиназы.
Compositions and Use of N-Chlorotaurine for Treatment and Prevention of Respiratory Infections
2022.09.01 US 2022273594 A1
Настоящее изобретение относится композициям и методам лечения и профилактики респираторных инфекций, включая вирусную инфекцию, например, коронавирус SARS-CoV-2 или его варианты. Методы включают введение терапевтически эффективного количества N-хлоротаурина (N-Chlorotaurine) (примерно от 0,1% до 1% раствора N-хлоротаурина в воде) путем назального распыления в ноздри, перорального распыления в горло и распыления в легкие с помощью небулайзера.
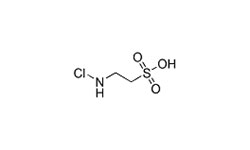
N-хлоротаурин - антиоксидант, обладает антимикробными свойствами.
Compound and method for the treatment of coronaviruses
2021.12.16 WO 2021250038 A1
Настоящее изобретение относится к применению клофоктола (Clofoctol) для лечения заболевания, вызванного коронавирусом, в частности Covid-19.
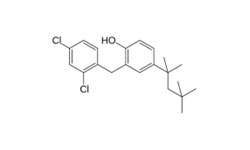
Клофоктол является бактериостатическим антибиотиком.
Cyclobenzaprine for use in the treatment of coronavirus
2022.11.17 WO 2022238886 A1
Настоящее изобретение относится к циклобензаприну (Cyclobenzaprine), его солям или метаболитам для применения в лечении заболеваний, связанных с коронавирусными инфекциями, в частности, к SARS-CoV-2. Показано, что EC50=4,1 мкМ, CC50=61,9 мкМ, SI=15,4.
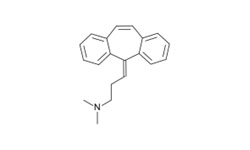
Циклобензаприн - миорелаксант центрального действия.
Antiviral Ruthenate(III) therapeutics
2021.10.07 WO 2021195763 A1
Изобретение относится к области медицины, в частности, к использованию транс-[тетрахлоробис (1H-индазол) рутената натрия(III)] (BOLD-100) для лечения вирусных заболеваний, в том числе, SARS-CoV-2. BOLD-100 - первый в своем классе противораковый препарат на основе рутения, с ограниченными побочными эффектами. Эсперименты на клетках Vero-E6 показали как до, так и послеинфекционную коронавирусную противовирусную эффективность BOLD-100 в модели SARS-CoV-2 in vitro с наномолярным ингибированием вирусной репликации в культуре клеток (относительная IC50 9,4 нМ и 15,6 нМ) и 50% снижением гибели вирусных клеток при низких микромолярных концентрациях (абсолютная EC50 1,8 мкМ и 1,9 мкМ.).
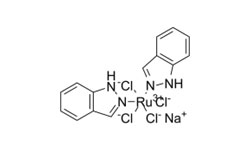
BOLD-100 (IT-139; KP-1339), или транс-[тетрахлоробис (1H-индазол)рутенат(III) натрия], - это противораковый терапевтический препарат на основе рутения, находящийся в стадии клинической разработки.
Compositions and methods for treating lung inflammation
2022.01.27 WO 2022020209 A1
Изобретение относится к области иммунобиологии, молекулярной биологии и медицины. Раскрыты методы и композиции, пригодные для использования при лечении инфекции или заболевания, вызванного респираторным вирусом (например, SARS-CoV-2), включающие введение субъекту, нуждающемуся в этом, антагониста рецептора нейрокинина 1 (NK1R), в частности, апрепитанта (Aprepitant) или его фармацевтически приемлемуой соли, сольвата, пролекарства.
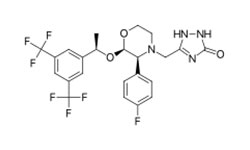
Апрепитант - противорвотное средство; селективный высокоаффинный антагонист рецепторов нейрокинина-1 субстанции Р.
Treatment for human coronavirus infection
2021.12.23 WO 2021257607 A1
Изобретение относится к лечению коронавирусной инфекции. Раскрываются методы использования ATN-161, нового антагониста интегринов α5β1 для лечения, облегчения или предотвращения инфекции или заболевания, вызванного коронавирусом SARS-CoV-2. Оценка терапевтического потенциала ATN-161 была проведена на линии клеток африканской зеленой мартышки VeroE6 с использованием компетентного вируса SARS-CoV-2. ATN-161 эффективно снижал вирусную нагрузку после заражения с оценкой IC50=3,16 мкМ.
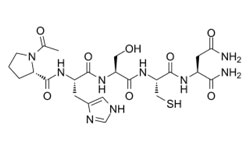
ATN-161 (L-Aspartamide, 1-acetyl-L-prolyl-L-histidyl-L-seryl-L-cysteinyl-) - это новый антагонист интегринов α5β1, который подавляет ангиогенез и рост метастазов печени в мышиной модели.
Compounds for use in the treatment of viral infections by respiratory syndrome-related coronavirus
2021.10.21 WO 2021209563 A1
Настоящее изобретение относится к соединению, выбранному из группы, состоящей из цинарина (Cynarine), эравациклина (Eravacycline) и прексасертиба (Prexasertib) или их фармацевтически приемлемых солей, предпочтительно эравациклина или фармацевтически приемлемой его соли, для применения в лечении и/или профилактике вирусных инфекций, вызванных бетакоронавирусами, особенно коронавирусами, связанными с респираторным синдромом, выбранными из видов "коронавирус, связанный с ближневосточным респираторным синдромом" (MERS-CoV) и "коронавирус, связанный с тяжелым респираторным синдромом" (SARS-CoV и SARS-CoV-2). Противовирусная активность была проверена на клетках Vero E6, инфицированных SARS-CoV-2. Цинарин, эравациклин и прексасертиб проявили выраженную ингибирующую активность против SARS-CoV-2 3CLpro со значениями IC50 1,815 мкМ, 1,645 мкМ и 1,996 мкМ соответственно.
Цинарин - желчегонное средство растительного происхождения, обладает также гепатопротекторным свойством, действие которого обусловлено свойствами входящих в состав полевого артишока биологически активных веществ.
Эравациклин — синтетический галогенированный антибиотик класса тетрациклинов фирмы Tetraphase Pharmaceuticals. Он обладает широким спектром активности, включая многие штаммы бактерий с множественной лекарственной устойчивостью.
Прексасертиб (LY2606368) - это низкомолекулярный ингибитор CHK1, исследуется эффективность прексасертиба в лечении острого миелоидного лейкоза, миелодиспластического синдрома, рабдомиосаркомы и медуллобластомы.
Efloxate for use as antiviral agent
2022.05.25 EP 4000614 A1
Настоящее изобретение относится к новому применению эфлоксата (Efloxate) в качестве противовирусного средства. Эфлоксат, его фармацевтически приемлемая соль, таутомер и/или сольват его или композиция, включающая его, могут применяться в профилактике и/или лечении инфекции коронавируса человека SARS-CoV-2. Согласно экспериментам, эфлоксат проявляет противовирусную активность в отношении коронавируса человека, включая SARS-CoV-2 в нецитотоксических концентрациях (12,5-50 мкМ), демонстрируя потенциал для использования в качестве лечения COVID-19.
Эфлоксат является сосудорасширяющим средством.
Efloxate for use as antiviral agent
2021.11.11 US 2021346403 A1
Настоящее изобретение предлагает применение соединения, нацеленного на минералокортикоидные рецепторы, для лечения COVID-19. Соединения являются антагонистами минералокортикоидных рецепторов, а именно, эплеренон (Eplerenone) или спиронолактон (Spironolactone). Эплеренон может назначаться в диапазоне 25-100 мг дважды в день, а спиронолактон назначается в диапазоне 25-100 мг/день. Частью настоящего изобретения является использование известных и безопасных лекарств, которые легко доступны, для лечения пациентов, которым грозит смерть от COVID-19.
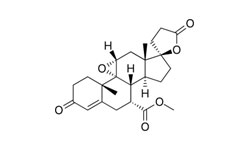
Эплеренон, продаваемый под торговой маркой Inspra, представляет собой калийсберегающий диуретик типа антагонистов альдостерона, который используется для лечения хронической сердечной недостаточности и высокого кровяного давления.
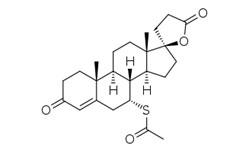
Спиронолактон, продающийся как Альдактон, Верошпирон и другие — калийсберегающий диуретик, конкурентный антагонист альдостерона и других минералокортикоидов. Применяется для лечения отёков при сердечной недостаточности, циррозе печени и заболеваниях почек.
Methods and uses of Halofuginone
2022.02.24 WO 2022040566 A1
Настоящее изобретение относится к лечению или профилактике заболевания, такого как COVID-19, у субъекта путем введения субъекту терапевтически эффективного количества галофугинона (Halofuginone) или его производного или фармацевтически приемлемой соли. Эксперименты показали, что галофугинон в 100 раз мощнее хлорохина и является мощным ингибитором инфекции SARS-CoV-2 со значениями IC50 в низком наномолярном диапазоне в нескольких моделях инфекции in vitro (IC50=349 нМ).
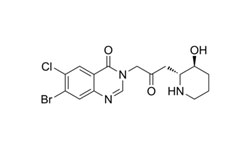
Галофугинон — синтетический аналог фебрифугина — алкалоида, первоначально выделенного из растения Dichroa febrifuga, является противопротозойным средством.
Treatment of ACE2-mediated viral infection
2022.12.01 WO 2022248738 A1
Настоящее изобретение относится к модуляции экспрессии ангиотензинпревращающего фермента 2 (ACE2) рецептором фарнезоида X (FXR). Предлагаются методы лечения заболевания, опосредованного ACE2, у человека и методы снижения восприимчивости человека к заболеванию, опосредованному ACE2, путем снижения активности или экспрессии рецептора фарнезоида X (FXR) у человека. ACE2-опосредованные заболевания включают инфекцию вирусами, связывающими ACE2, такими как SARS-CoV-2. Активность или экспрессия FXR может быть снижена путем введения ингибитора FXR, такого как Z -гуггулстерон (Z-Guggulsterone, ZGG) или урсодезоксихолевая кислота (Ursodeoxycholic acid, UDCA). Было продемонстрировано, что ингибирование FXR с помощью утвержденного препарата урсодезоксихолевой кислоты (UDCA) или безрецептурного фитостероида Z-гуггулстерона (ZGG) снижает экспрессию ACE2 и инфекцию SARS-CoV-2 in vitro и in vivo. Это открывает новые возможности для профилактики и терапии инфекции SARS-CoV-2.
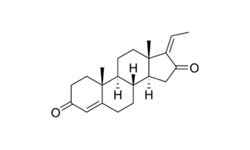
Z-Гуггулстерон - это фитостероид, содержащийся в смоле растения Commiphora mukul, ингибирует ангиогенез in vitro и in vivo; оказывает противовоспалительное действие.
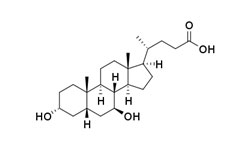
Урсодезоксихолевая кислота — лекарственный препарат гепатопротекторного действия.
Antiviral applications of Picolinic acid and its derivatives
2022.07.28 WO 2022157656 A1
Настоящее изобретение представляет методы ингибирования проникновения вируса в клетку-хозяина с помощью пиколиновой кислоты или ее соли или производного. Предлагаются методы лечения или предотвращения вирусной инфекции у субъекта путем введения пиколиновой кислоты (picolinic acid) или ее соли или производного. Эти методы эффективны в отношении SARS-CoV-2, вируса гриппа А, вируса парагриппа человека, вируса простого герпеса, вируса японского энцефалита, вируса Зика или флавивирусной инфекции.Результаты экспериментов показывают, что пиколиновая кислота проявляет значительную противовирусную активность против SARS-CoV-2 (IC50=2 мкМ). как в линиях клеток различных видов, так и в доклинической модели на животных.
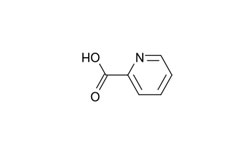
Пиколиновая кислота (PCL-016) - это метаболит триптофана; действует как противоинфекционное и иммуномодулирующее средство; как природный продукт содержится в Aloe africana, Saccharomyces cerevisiae.
Methods of treating and preventing coronavirus infections using inhibitors of coagulation factor Xa
2021.10.14 WO 2021207031 A1
Настоящее изобретение относится к способам лечения и/или профилактики коронавирусных инфекций с использованием одного или нескольких ингибиторов фактора свертывания крови Xa, а именно, ривароксабана (Rivaroxaban), апиксабана (Apixaban), эдоксабана (Edoxaban) и/или бетриксабана (Betrixaban).
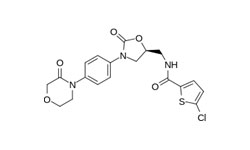
Ривароксабан — пероральный антикоагулянт из группы прямых ингибиторов фактора Xa. В частности, он используется для лечения тромбоза глубоких вен и легочной эмболии.
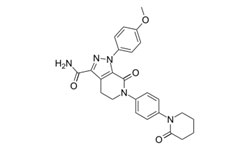
Апиксабан — антикоагулянт, прямой ингибитор фактора свёртываемости крови Ха, используется для лечения и предотвращения образования тромбов и предотвращения инсульта у людей с неклапанной фибрилляцией предсердий.
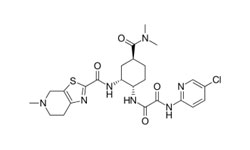
Эдоксабан, продаваемый, среди прочего, под торговой маркой Lixiana, является антикоагулянтным препаратом и прямым пероральным ингибитором фактора Ха.
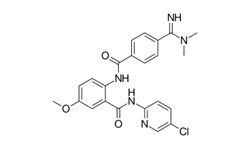
Бетриксабан - пероральный антикоагулянт, прямой ингибитор фактора свертывания Xa, применяется для профилактики венозной тромбоэмболии в условиях умеренной и тяжёлой ограниченной подвижности пациентов.
Use of Berbamine or its Analogue for Preventing or Treating RNA Virus Infection
2022.12.01 US 2022378778 A1
Настоящее изобретение относится к способу предотвращения или лечения субъекта, страдающего от флавивирусной инфекции, путем введения субъекту эффективного количества бербамина (Berbamine) или его аналога, где флавивирусная инфекция вызвана вирусом японского энцефалита, вирусом Зика или вирусом Денге. Изобретение также предоставляет способ предотвращения или лечения субъекта, страдающего от коронавируса, в частности, коронавируса SARS-CoV-2 или MERS-CoV. Изобретатели оценили анти-SARS-CoV-2 активность бербамина в клетках Vero-E6 и обнаружили, что бербамин значительно ингибировал выход вируса, как было определено с помощью анализа qRT-PCR (EC50~2,3 мкМ) или анализа титрования вируса (EC50~4,7 мкМ). Индекс селективности бербамина (CC50/EC50) составил 48,9. В целом, эти данные свидетельствуют о том, что бербамин является потенциальным препаратом против SARS-CoV-2 и MERS-CoV. Бербамин - блокатор кальциевых каналов; также проявляет антигипертензивное, антиаритмическое и противовоспалительное действие; исследовался для лечения хронической миелоидной лейкемии, поскольку продемонстрировал значительный антипролиферативный эффект в отношении опухолевых клеток.
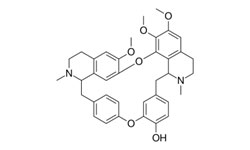
Бербамин - бис-бензилизохинолиновый алкалоид, широко используемый в традиционной китайской медицине.
Methods for treating or preventing a viral infection or inhibiting viral replication
2021.11.04 WO 2021219495 A1
В настоящем документе представлены композиции и методы лечения или профилактики вирусных инфекций, включая коронавирусную болезнь (COVID-19), с использованием далцетрапиба (Dalcetrapib), аналога далцетрапиба или фармацевтически приемлемой соли, гидрата или сольвата. Установлено, что дальцетрапиб ингибирует ферментативную активность основной протеазы 3CL SARS-CoV-2 с IC50=14,4 мМ.
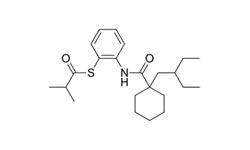
Далцетрапиб — ингибитор CETP, который разрабатывался компанией Hoffmann-La Roche, препарат был направлен на повышение уровня холестерина ЛПВП в крови.
Methods of treating viral infections using inhibitors of nucleotide synthesis pathways
2021.09.23 WO 2021189018 A1 (A9)
Изобретение представляет методы лечения вирусных инфекций, таких как COVID-19, с помощью агента, который ингибирует путь синтеза нуклеотидов, в частности, ингибитора дигидрооротатдегидрогеназы бреквинара (Brequinar). Бреквинар предоставляется субъекту в соответствии с режимом дозирования, который подбирает уровни препарата в легких для достижения оптимального терапевтического эффекта. Изобретение также представляет комбинированные методы лечения, в которых ингибитор дигидрооротатдегидрогеназы вводится вместе со вторым терапевтическим агентом, например, с ремдесивиром. В экспериментах бреквинар продемонстрировал IC50=0,2 мкМ, EC50 ~0,2мкМ, EC90=0,345 мкМ, что указывает на мощную анти-SARS-CoV-2 активность.
Бреквинар — это препарат, который действует как сильнодействующий и селективный ингибитор фермента дигидрооротатдегидрогеназы. Он блокирует синтез нуклеотидов на основе пиримидина в организме и, таким образом, подавляет рост клеток.
Viral entry inhibitors and RNA polymerase inhibitors
2021.10.07 WO 2021203055 A1
Настоящее изобретение относится к ингибиторам проникновения вирусов и ингибиторам РНК-полимеразы, фармацевтическим композициям, включающим один или несколько из них, и комбинированным препаратам, а также к способам получения и применения вышеуказанных препаратов для лечения определенных заболеваний. Ингибиторы вирусного проникновения настоящей заявки могут применяться для лечения заболеваний, вызванных SARS-CoV, вирусом Эбола, MERS-CoV и другими вирусами. В частности, рассматривается ингибитор цистеиновой протеазы K11777 и его фармацевтически приемлемые соли. Эксперименты показали,что на клеточной линии Vero E6 EC50=0,62 мкМ, CC50>10 мкМ. Соотношение EC50 /CC50, т.е. терапевтический индекс, указывает на то, что K11777 не только потенциально эффективен для лечения и/или профилактики инфекции SARS-CoV-2, но и безопасен. Его терапевтическими мишенями являются цистеиновая протеаза простейшего паразита Trypanosoma cruzi и катепсины B и L, которые связаны с прогрессированием рака.
K-11777, также известный как APC 3316 и K 777, является мощным, необратимым ингибитором цистеиновых протеаз и мощным и селективным антагонистом CCR4.
Treatment of COVID-19 with a sine compound
2021.10.07 WO 2021202745 A1
Настоящее раскрытие относится к способу лечения COVID-19 у нуждающегося в этом субъекта, включающему введение субъекту терапевтически эффективного количества соединения SINE (Selective Inhibitor of Nuclear Export) или его фармацевтически приемлемой соли. COVID-19 может быть в тяжелой форме, субъект может быть взрослым в возрасте 18 лет или старше, соединение SINE может быть селинексором (Selinexor), который назначается перорально в дозе около 20 мг на дозу или 40 мг на дозу. В экспериментах на клеточной линии Vero E6 селинексор продемонстрировал IC90 < 10 нМ.
Селинексор (selinexor, KPT-330) - противораковый препарат американской фармацевтической компании Karyopharm Therapeutics, представляет собой селективный ингибитор ядерного экспорта, разрабатывается для лечения пациентов с множественной миеломой.
Method for treatment of COVID-19-associated conditions
2021.09.16 US 2021283152 A1
Настоящее раскрытие относится к методам лечения ассоциированных с COVID-19 заболеваний. В частности, метод может включать введение фостаматиниба (Fostamatinib) или фармацевтически приемлемой соли пациенту с коронавирусной инфекцией или подозрением на нее, например, COVID-19, коронавирусом, ассоциированным с тяжелым острым респираторным синдромом (SARS-CoV) или коронавирусом, ассоциированным с ближневосточным респираторным синдромом (MERS-CoV). В клинических испытаниях по сравнению с группой плацебо, в группе фостаматиниба оказался значительно меньший процент пациентов с развитием тяжелого или критического заболевания, требующих интенсивной терапии, в течение 29 дней после приема первой дозы исследуемого препарата.
Фостаматиниб (R-788, NSC-745942, R-935788) — пероральный лекарственный препарат для лечения хронической иммунной тромбоцитопении, селективный низкомолекулярный ингибитор киназы Syk.
Application of benflumetol and derivatives thereof in treatment of coronavirus infection
2022.07.01 TW 202224673 A
Настоящее изобретение относится к применению бенфлуметола (Benflumetol) и его фармацевтически приемлемой соли, сольвата или гидрата при приготовлении лекарственных средств. Препараты используются для лечения заболеваний или инфекций, вызванных коронавирусом (предпочтительно SARS-CoV-2). Результаты эксперимента по ингибированию пролиферации вируса показали, что тестируемое соединение может эффективно ингибировать репликацию вирусного генома SARS-CoV-2 при концентрациях 100 мкМ, 50 мкМ и 25 мкМ. Результаты по исследованию цитотоксичности показали, что обработка испытуемым соединением (бенфлуметолом) не изменяла жизнеспособность клеток при всех испытанных концентрациях, то есть испытуемое соединение не оказывало токсического действия на клетки при всех концентрациях.
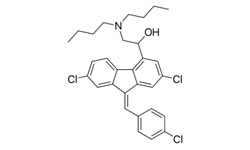
Бенфлуметол или Люмефантрин — противомалярийный препарат, используемый в сочетании с Артеметером.
Application of propranolol in resisting coronavirus infection
2022.07.15 CN 114748458 A
Изобретение раскрывает применение пропранолола (Propranolol) и его производных или фармацевтически приемлемых солей в приготовлении лекарственных средств для профилактики или лечения коронавирусной инфекции. Исследования показывают, что пропранолол может эффективно ингибировать или разрушать органеллы репликации вируса и ингибировать репликацию вируса, обладает явным и заметным эффектом профилактики и резистентности к коронавирусам, включая SARS-CoV-2, SARS-CoV и MERS-CoV, и может облегчать различные последствия коронавируса. Изобретение также раскрывает применение пропранолола и его производных или его фармацевтически приемлемых солей в приготовлении лекарственных средств для профилактики или лечения коронавирусной инфекции в сочетании с другими лекарственными средствами. После комбинированного применения вирусная нагрузка может быть явно снижена при низкой дозировке.

Пропранолол — неселективный β-адреноблокатор, антагонист 5-HT1A-рецепторов; оказывает антиангинальное, антиаритмическое, утеротонизирующее, гипотензивное действие.
Application of DH404 in treatment of SARS-CoV-2 infection
2022.06.14 CN 114617890 A
Изобретение относится к применению DH404 или его фармацевтически приемлемой соли в приготовлении лекарственных средств для лечения заболеваний, связанных с ангиотензинпревращающим ферментом 2 (ACE2), в частности, для профилактики и лечения новой коронавирусной пневмонии (COVID -19). Было обнаружено, что соединение DH404 может оказывать сильное ингибирующее действие на основной рецептор ACE2 вируса SARS-CoV-2, обладает, низким уровнем токсичности и побочных эффектов, хорошей безопасностью и может быть использовано в качестве клинико-профилактическое средства для облегчения и/или лечения COVID-19/SARS-CoV-2. Согласно результатам эксперимента, DH404 ингибировал экспрессию белка ACE2 на модели клеток рака легкого на 40%, 50% и 70% при концентрациях 0,625, 1,25 и 2,5 мкМ соответственно.
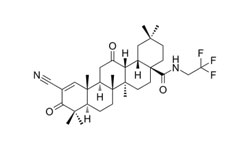
DH404 (Dihydro-CDDO-trifluoroethyl amide, CDDO-dhTFEA) - представляет собой синтетическое тритерпеноидное соединение, предположительно является новым активатором Nrf2 с терапевтическим потенциалом при сердечных заболеваниях за счет подавления окислительного стресса.
Application of GN44028 in treatment of SARS-CoV-2 infection
2022.06.10 CN 114601827 A
Изобретение относится к применению GN44028 или его лекарственной соли для приготовления лекарственных средств для профилактики и лечения заболеваний, связанных с ангиотензинпревращающим ферментом 2 (ACE2), а именно, COVID-19/SARS-CoV-2. Обнаружено, что соединение GN44028 неожиданно может оказывать сильное ингибирующее действие на вирус SARS-CoV-2 и обладает низким уровнем токсичности и побочных эффектов и хорошей безопасностью. В тестах активности для ингибирования внутриклеточной экспрессии белка ACE2 экспрессия белка ACE2 в клетках ингибируется на 35% и 50% при концентрации GN44028 2,5 мкМ и 5,0 мкМ соответственно.
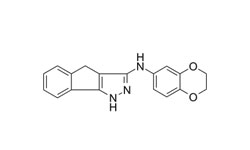
GN44028 представляет собой мощный и активный при пероральном приеме ингибитор фактора HIF-1α, индуцируемого гипоксией; может использоваться в исследованиях рака.
Application of chicoric acid in treatment of SARS-CoV-2 infection
2022.06.10 CN 114601820 A
Изобретение относится к применению цикориевой кислоты (Chicoric acid), ее лекарственных солей или растений, содержащих цикориевую кислоту, для приготовления лекарственных средств для профилактики и лечения заболеваний, связанных с ангиотензинпревращающим ферментом 2 (ACE2), в частности, для профилактики и лечения новой коронавирусной пневмонии (COVID-19). Результаты экспетимента показали, что 2 мкМ цикориевой кислоты могут снижать экспрессию белка ACE2 в клетках более чем на 50%.
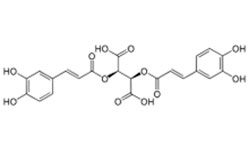
Цикориевая кислота - соединение, способное усиливать высвобождение инсулина и поглощение глюкозы, является новым потенциальным антидиабетическим средством, обладающим свойствами как сенсибилизирующих инсулин, так и секретирующих инсулин.
Application of CAY10603 in preparation of drugs for preventing and treating coronavirus-related diseases
2022.05.05 WO 2022088038 A1
Данное изобретение раскрывает применение CAY10603 или его фармацевтически приемлемой соли, его изотопа, его стереоизомера, смеси его стереоизомеров, его таутомера, его сложного эфира, его амида или его пролекарства в приготовлении лекарственных средств для профилактики и лечения заболеваний, вызванных коронавирусами. Описанными коронавирусами являются SARS-Cov-2, SARS-CoV, HCoV 229E, NL63, OC43, HKU1 и MERS-CoV. Впервые подтверждено, что CAY10603 оказывает ингибирующее действие на SARS-Cov-2, имеет низкое среднее значение эффективной концентрации и большой потенциал применения. EC50 CAY10603 составляет около 13,5±9,4 мкМ.
CAY10603 (BML-281) является селективным ингибитором HDAC6, проявляет потенциальную противоопухолевую активность.
Application of ITF2357 in preparation of medicine for preventing and treating coronavirus
2022.05.06 CN 114432287 A
Изобретение относится к области медицины и, в частности, касается применения ITF2357 (Givinostat) или его фармацевтически приемлемой соли, изотопа, стереоизомера, смеси стереоизомеров, таутомера, сложного эфира, амида или пролекарства в приготовлении лекарственных средств для профилактики и лечения заболеваний, вызванных коронавирусом. Коронавирус представляет собой SARS-Cov-2, SARS-CoV, HCoV 229E, NL63, OC43, HKU1 и MERS-CoV. Заболевания, вызванные коронавирусом, представляют собой пневмонию или осложнения пневмонии, вызванной любым из вирусов SARS-Cov-2, SARS-CoV, HCoV 229E, NL63, OC43, HKU1 или MERS-CoV. Впервые подтверждено, что ITF2357 оказывает ингибирующее действие на новый коронавирус, имеет низкое среднее значение эффективной концентрации и большой потенциал применения. EC50 ITF2357 составляет около 6,8±1,0 мкМ.
ITF2357 (Гивиностат) является перорально активным ингибитором гистондеацетилазы (HDAC) с потенциальной противовоспалительной, антиангиогенной и противоопухолевой активностью.
Application of SIRTINOL in preparation of medicine for preventing and treating coronavirus
2022.05.06 CN 114432283 A
Изобретение раскрывает применение сиртинола (Sirtinol) или его фармацевтически приемлемой соли, изотопа, стереоизомера, смеси стереоизомеров, таутомера, сложного эфира, амида или пролекарства в приготовлении лекарственных средств для профилактики и лечения заболеваний, вызванных коронавирусом. Коронавирус представляет собой SARS-Cov-2, SARS-CoV, HCoV 229E, NL63, OC43, HKU1 и MERS-CoV. Впервые подтверждено, что сиртинол оказывает ингибирующее действие на новый коронавирус, имеет низкое среднее значение эффективной концентрации и большой потенциал применения. EC50 сиртинола составляет около 82,9±61,1 мкМ.
Сиртинол является специфическим ингибитором SIRT1 и SIRT2.
Application of panobinostat in preparation of medicine for preventing and treating coronavirus
2022.05.06 CN 114432303 A
Изобретение раскрывает применение панобиностата (Panobinostat) или его фармацевтически приемлемой соли, изотопа, стереоизомера, смеси стереоизомеров, таутомера, сложного эфира, амида или пролекарства в приготовлении лекарственных средств для профилактики и/или лечения заболеваний, вызванных корона вирус. Коронавирус представляет собой SARS-Cov-2, SARS-CoV, HCoV 229E, NL63, OC43, HKU1 и MERS-CoV. Впервые подтверждено, что панобиностат оказывает ингибирующее действие на новый коронавирус, имеет низкое среднее значение эффективной концентрации и большой потенциал применения. EC50 панобиноста составляет около 2,8±1,0 мкМ.
Панобиностат, продаваемый под торговой маркой Фаридак, представляет собой лекарство, используемое для лечения множественной миеломы, действует как неселективный ингибитор гистондеацетилазы.
Application of Tannic acid in preparation of anti-respiratory virus drug
2022.02.24 WO 2022036774 A1
Изобретение относится к области биомедицины. Раскрывается применение дубильной кислоты (Tannic acid) в приготовлении противовирусного препарата. Эксперименты с живыми вирусами показывают, что дубильная кислота оказывает значительное ингибирующее действие и определенное лечебное действие на респираторные вирусы, такие как коронавирусы, включающие вирусы SARS-CoV-2 и гриппа A H1N1, и имеет широкую перспективу применения в области получения противовирусных препаратов. Дубильная кислота содержится в различных растениях и является естественным активным соединением, существующим в природе; кроме того, дубильная кислота также используется в качестве пищевой добавки, обладает высокой безопасностью и обеспечивает хорошую основу для разработки лекарств. В эксперименте дубильная кислота показала высокую активность против вируса SARS-CoV-2, ее значение IC50 против вируса SARS-CoV-2 составило 0,0032 мкМ. Cинтезируется большим количеством растений; исторически использовалась для лечения диареи, местно для обработки кожных ожогов и ректально для лечения неуточненных заболеваний прямой кишки.
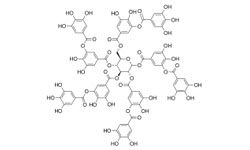
Дубильная кислота представляет собой встречающийся в природе растительный полифенол, одна из форм танинов.
Pannexin-1 inhibitors for the treatment of SARS-CoV-2 infected COVID-19 patients with or without an associated acute respiratory syndrome
2021.11.04 WO 2021220137 A2
Настоящее изобретение относится к применению ингибитора паннексина-1 пробенецида (Probenecid) для лечения новой коронавирусной инфекции с сопутствующим острым респираторным синдромом или без него. Пробенецид можно вводить либо отдельно, либо в комбинации с лекарственными средствами, препятствующими репликации вируса, такими как, но не ограничиваясь ими, ингибиторы РНК-зависимой РНК-полимеразы, или с лекарственными средствами, препятствующими гипервоспалению легких, такими как, но не ограничиваясь ими, ингибиторы пути IL-6. Настоящее изобретение включает также применение пробенецида в сочетании с кверцетином или галлатом эпигаллокатехина (EGCG) в количестве, эффективном для лечения коронавирусной инфекции у человека. Пробенецид можно вводить перорально, инъекционно, аэрозольно, интраназально. Доказано действие пробенецида в отношении нескольких штаммов вируса SARS-CoV-2, где процентное ингибирование репликации вируса составляет 55,3, 53,7, 37,5 и 59,2 для IHUMI 3, IHUMI 845, IHUMI 2137 и UK штаммов соответственно при концентрации пробенецида 10 мкМ и процентное ингибирование репликации вируса составляет 80,2, 9,9 и 48,1 для вирусных штаммов IHUMI 3, IHUMI 2096 и IHUMI 2137 соответственно при концентрации пробенецида 1 мкМ.
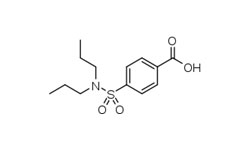
Пробенецид, также продаваемый под торговой маркой Пробалан, представляет собой лекарство, которое увеличивает выделение мочевой кислоты с мочой. Он в основном используется при лечении подагры и гиперурикемии.
Use of Bacitracin a in preparation of drugs for preventing and treating coronaviruses
2021.10.14 WO 2021203704 A1
В настоящем изобретении раскрывается применение бацитрацина А или его фармацевтически приемлемых солей, изотопов, стереоизомеров, смесей стереоизомеров, таутомеров, сложных эфиров, амидов или пролекарств для приготовления лекарственных средств для профилактики и/или лечения заболеваний, вызванных коронавирусами. Коронавирусы представляют собой новые коронавирусы SARS-CoV-2, SARS-CoV, HCoV 229E, NL63, OC43, HKU1 и MERS-CoV. Бацитрацин активен против грамположительных микроорганизмов, таких как бета-гемолитические стрептококки, стафилококки, и некоторых грамотрицательных патогенов.
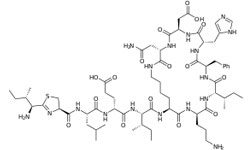
Бацитрацин — полипептидный антибиотик, производимый штаммами бактерии Bacillus subtilis, ингибирует синтез клеточной оболочки бактерий.
Use of Carglumic acid in preparation of drugs for preventing and treating coronaviruses
2021.10.14 WO 2021203703 A1
Раскрыто применение карглуминовой кислоты (Carglumic acid) или ее фармацевтически приемлемых солей, изотопов, стереоизомеров, смесей стереоизомеров, таутомеров, сложных эфиров, амидов или их пролекарств в приготовлении препаратов для профилактики и/или лечения заболеваний, вызванных коронавирусами. Коронавирусы представляют собой новые коронавирусы SARS-Cov-2, SARS-CoV, HCoV 229E, NL63, OC43, HKU1 и MERS-CoV. Карглуминовая кислота в экспериментах показала значительную активность против SARS-Cov-2 (EC50=13,92 мкМ) при низкой токсичности.
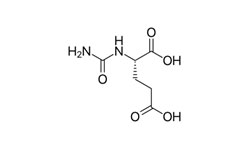
Карглуминовая кислота, продаваемая, в частности, под торговой маркой Carbaglu, используется для лечения гипераммониемии; карглуминовая кислота является активатором карбамоилфосфатсинтетазы 1 (CPS 1).
Application of diphyllin in preparation of anti-novel coronavirus drugs
2021.08.13 CN 113244223 A
Изобретение относится к области биомедицины, а именно, касается использования дифиллина (Diphyllin) или его соли, или его стереоизомера, или его сольвата для приготовления препаратов против нового коронавируса. Исследования показывают, что дифиллин оказывает хорошее ингибирующее действие на псевдовирус SARS-CoV-2 и истинный вирус, может эффективно противостоять инфекции псевдовируса SARS-CoV-2 и истинного вируса и имеет отличные перспективы применения. Дифиллин является основным компонентом экстракта листьев лотоса традиционной китайской медицины., который обладает противораковой и противовоспалительной активностью, является эффективным ингибитором ВИЧ-1, а его побочные эффекты относительно невелики.
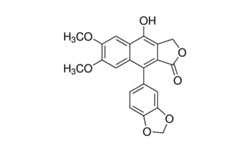
Дифиллин природное соединение, извлекаемое из тропических растений, имеющих особое значение в традиционной китайской медицине.
Application of corilagin in inhibition of coronavirus replication to play roles of anti-coronavirus drugs
2021.03.09 CN 112451534 A
Изобретение раскрывает применение корилагина (Corilagin) или его фармацевтически приемлемой соли для ингибирования репликации коронавируса в качестве противокоронавирусных препаратов. В соответствии с изобретением эксперименты доказывают, что корилагин может эффективно ингибировать репликацию SARS-CoV-2 in vitro, оказывает противокоронавирусное действие на SARS-CoV-2 путем ингибирования РНК-зависимой РНК-полимеразы и имеет важные перспективы применения для лечения коронавирусной инфекции. Корилагин проявлял дозозависимое ингибирующее действие на SARS-CoV-2 со значением EC50=0,131 мкМ.
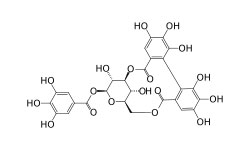
Корилагин представляет собой полифенол, содержащийся в растительных препаратах традиционной китайской медицины; сообщается, что он обладает противовоспалительными и противоопухолевыми свойствами.
Application for liquiritin and derivatives of liquiritin in preparation of drugs for treating and/or preventing novel coronaviruses
2020.06.19 CN 111297882 A
Изобретение относится к области фармации и касается применения ликвиритина (Liquiritin), его фармацевтически приемлемых солей и производных при приготовлении противокоронавирусных препаратов для лечения и/или профилактики. В соответствии с изобретением обнаружено, что ликвиритин способен эффективно ингибировать новые коронавирусы SARS-CoV-2 на клеточном уровне, ЕС50 составляет 2,39 мкМ. Ликвиритин оказывает положительное влияние на лечение и/или профилактику новых коронавирусов SARS-CoV-2. Ликвиритин эффективно ингибирует метаболизм прогестерона, опосредованный AKR1C1, in vivo. Ликвиритин действует как антиоксидант и обладает нейропротекторной, противораковой и противовоспалительной активностью.
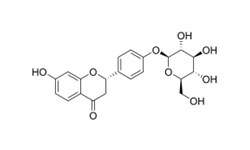
Ликвиритин, флавоноид, выделенный из Glycyrrhiza uralensis (солодка), является мощным и конкурентоспособным ингибитором AKR1C1.
Аналитические материалы в интересах (по заказам) органов государственной власти.
Подготовлены в рамках Дополнительного соглашения к Соглашению о предоставлении субсидии из федерального бюджета на финансовое обеспечение выполнения государственного задания на оказание государственных услуг (выполнение работ) (№ 075-ГЗ/Ц1960/401/2) № 075-03-2021-485/2 от 19 октября 2021 г., номер государственного учета научно-исследовательской, опытно-конструкторской и технологической работы гражданского назначения 121102900156-6 от 27 октября 2021 г.).Читать
 (C) Коллектив авторов, 2022.
(C) Коллектив авторов, 2022.
Аналитические материалы в интересах (по заказам) органов государственной власти.
Подготовлены в рамках Дополнительного соглашения к Соглашению о предо-ставлении субсидии из федерального бюджета на финансовое обеспечение выполнения государственного задания на оказание государственных услуг (выполнение работ) № 075-03-2022-467/1 от 28 июля 2022 года, номер госу-дарственного учета научно-исследовательской, опытно-конструкторской и технологической работы гражданского назначения 121102900156-6 от 27 ок-тября 2021 г.).Читать
 (C) Коллектив авторов, 2023.
(C) Коллектив авторов, 2023.
Аналитические материалы в интересах (по заказам) органов государственной власти.
Подготовлены в рамках Дополнительного соглашения к Соглашению о предоставлении субсидии из федерального бюджета на финансовое обеспечение выполнения государственного задания на оказание государственных услуг (выполнение работ) № 075-03-2023-663/2 от 11 августа 2023 года, номер государственного учета научно-исследовательской, опытно-конструкторской и технологической работы гражданского назначения 121102900156-6 от 27 октября 2021 г. – проект № FGFM-2021-0004.Читать
 (C) Коллектив авторов, 2024.
(C) Коллектив авторов, 2024.


